各国药典纯化水标准
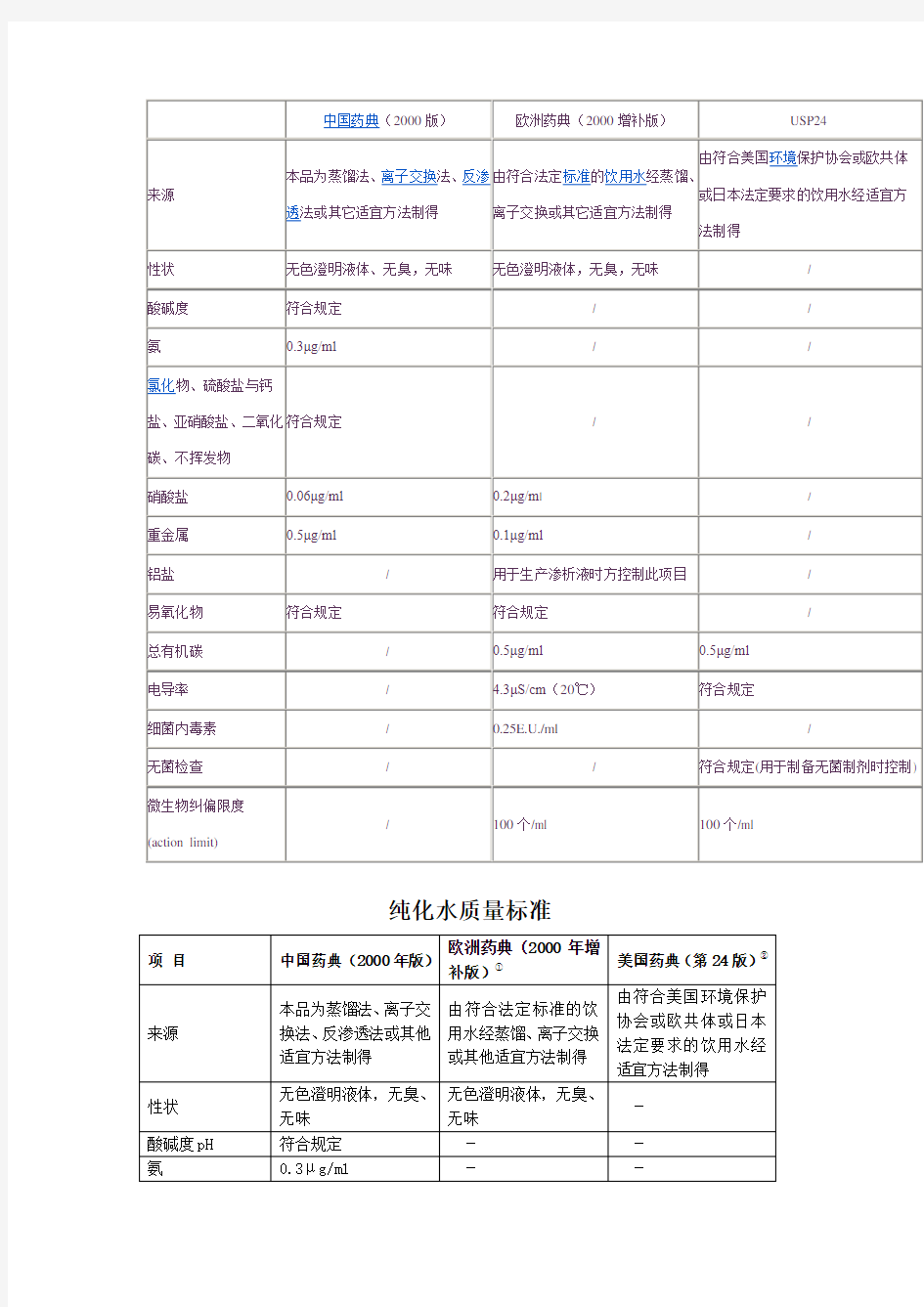

纯化水质量标准
世界上最早由国家颁布的药典正式版
《世界上最早由国家颁布的药典》 参考答案一: 世界上最早由国家颁布的药典是? 《唐本草》。 是我国隋唐时期的《新修本草》,又称《唐本草》。书成于公元659年(唐显庆四年), 共54卷,载药850种。市第一部官修药典性本草,比公元1546年问世的欧洲纽伦堡药典《科德药方书》早887年。 最早的《药典》――公元659年,唐代朝廷颁行《新修本草》。这是最早由国家制定的药典,比世界著名的1546年《纽伦堡药典》早9个世纪。 参考答案二: 世界上最早由国家颁布的药典是哪一个朝代?什么人制订的? 据历史记载;世界上最早由国家颁布的药典是公元657年唐政府组织苏敬等二十余人群 众编修本草,于公元659年完稿,名为《唐新修本草》(又名《唐本草》)。这是中国古代由 政府颁行的第一部药典,也是世界上最早的国家药典。它比欧洲纽伦堡政府公元1542年颁行 的《纽伦堡药典》早883年。该书共54卷,包括本草、药图、图经三部分,载药850种, 逐渐被传到欧洲和中国的邻国如日本、朝鲜、新加坡等,在国外得到广泛流传和应用。可惜如今没有图录记载。 参考答案三: 我国最早的一部药典是哪一部? 《新修本草》是在公元659年由唐代苏敬等20余人编写的我国政府颁行的第一部药典。它比欧洲最早的《佛罗伦萨药典》(1498年出版)早839年,比1535年颁发的世界医学史 上有名的《纽伦堡药典》早876年,比俄国第一部国家药典(1778年颁行)早1119年,因 此有世界第一部药典之称。 原书是卷子本,计21卷。除序例外,以玉石、草木、兽禽、虫鱼、果菜、米谷等分类, 共收集药品859种,并注意药物实际形态。当时曾下诏全国,征询各地药物形色,画成图形,另外还加有说明的图经。《新修本草》的药图和图经的篇幅繁富,超过正文的资料。
美国药典简介
美国药典简介 1. 标题和修订(Title and Revision). 9 2. 药典地位和法律认可(Official status and legal recognition)9 2.10 药典正文(Official Text) 9 2.20 药典物品(Official Articles). 9 2.30 法律认可(Legal Recognition). 10 3. 与标准的符合性(Conformance to standard). 10 3.10 标准的适用性(Applicability of standard) 10 3.10.10 制剂、原料药、辅料的标准的适用性(Applicability of Standards to Drug Products, Dru g Substances, and Excipients). 10 3.10.20 医疗器械、营养补充剂、以及其组成成分的标准的适用性(Applicability of Standards to Medical Devices, Dietary Supplements, and Their Components and Ingredients)11 3.20 一致性的标示(Indicating Conformance). 11 4. 药典各论和通则(Monographs and general chapters)12 4.10 各论(Monographs) 12 4.10.10 检测程序的适用性(Applicability of Test Procedures) 12 4.10.20 接受标准(Acceptance Criteria) 12 4.20 附录(General Chapter). 12 5. 各论组成(Monograph Components). 13 5.10 分子式(Molecular formula). 13 5.20 附加物质、赋形剂、组分(Added Substances, Excipients, and Ingredients) 13 5.20.10官方原料药中附加的物质、赋形剂、组分(Added Substances, Excipients, and Ingredien ts in Official Substances). 13 5.20.20官方制剂中的附加物质、赋形剂、组分(Added Substances, Excipients, and Ingredients in Official Products). 13 5.30 性状和溶解性(Description and Solubility). 14
各国对中药的质量要求
②植物油脂和提取物部分: ③成方制剂和单味制剂:所有胶剂一般应检查总灰分、重金属、砷盐、微生物限度。 二、国外 ①、法国、德国、英国: 重金属及砷盐限量: 砷(As)食品总量≤1 mg/kg,草药≤5 mg/kg。 铅(Pb)食品总量≤1 mg/kg,草药≤5 mg/kg。 锡(Sn)食品总量≤200mg/kg, 铜(Cu)食品总量≤20mg/kg,茶≤150mg/kg。 锌(Zu)食品总量≤50mg/kg。 ②、加拿大: 重金属及砷盐限量: 1、草药材: 铅(Pb)≤10 mg/kg;铬(Cr)≤ 0.2 mg/kg。 镉(Cd) ≤0.3 mg/kg;砷(As)≤ 5 mg/kg。 汞(Hg)≤ 0.2 mg/kg。 2、草药产品: 铅(Pb)≤0.02 mg/day;铬(Cr)≤ 0.006 mg/day。 镉(Cd) ≤0.02 mg/day;砷(As)≤ 0.01 mg/day。 汞(Hg)≤ 0.02 mg/day。 ③、美国: 重金属及砷盐限量: 适用范围:草药 重金属总量10-20 mg/kg;铅(Pb)3-10 mg/kg。
汞(Hg)<3 mg/kg;砷(As)<3 mg/kg 重金属及砷盐限量: 适用范围:饮食补充剂 1、饮食补充剂原料: 铅(Pb)≤10 mg/kg;铬(Cr)≤ 0.2 mg/kg。 镉(Cd) ≤0.3 mg/kg;砷(As)≤ 5 mg/kg。 2、饮食补充剂产品: 铅(Pb)≤0.02 mg/day;铬(Cr)≤ 0.006 mg/day。 镉(Cd) ≤0.02 mg/day;砷(As)≤ 0.01 mg/day。 汞(Hg)≤ 0.02 mg/day。 ④、WHO(世界卫生组织): 重金属及砷盐限量: 适用范围:草药 铅(Pb)≤10 mg/kg;镉(Cd)≤0.3 mg/kg。 重金属限量(毫克/公斤) 铅Pb≤5.0 mg/kg 镉Cd ≤0.2 mg/kg 汞Hg ≤0.1 mg/kg 据不完全统计,有30%中草药的重金属和农药残留量不符合标准,其中有:川芎、细辛、白花蛇舌草、白头翁、蒲公英、菟丝子、茵陈、泽泻、地骨皮、枇杷叶、桂枝、猪苓、山茱萸、夜交藤、徐长卿、红花等。重金属超标的中成药品种有牛黄解毒片、六神丸、天仙丸、追风透骨丸、天王补心丸、牛黄降压丸等。 ⑤、日本、韩国: 2009年日本、韩国相继公布了新的中药材重金属与农残许可标准与检测方法,并于2009年正式实行。这是继2005年日本、韩国对中药材二氧化硫的限量要求和检测方法以来对中药材的又一新规定。 新规定明确植物性中药材重金属标准是: (1)铅≤5mg/kg,砷≤3mg/kg,汞≤0.2mg/kg,镉≤0.3mg/kg。 (2)鹿茸的砷≤3mg/kg。 (3)以生药的萃取物和只用生药为主成分的制剂的总重金属为30mg/kg以下。但是含有矿物性生药时除外。 据报道,韩方对生药及其提取物和制剂实施的新标准,涉及品种占到中国对韩国中药出口的70%左右。韩国在2008年4月7日正式实施的中药材霉菌(aflatoxin)B1许可标准涉及中药材甘草、决明子、桃仁、半夏、柏子仁、槟榔、酸枣仁、远志、红花等九个品种。按照该标准,上述九种中药材霉菌B1必须低于10μg/kg(10ppm)。
美国药典中的药品存储条件
美国药典中的药品存储条件-Temperature and storage definitions 在日常工作中,经常有很多同学被药品存储条件的字面意思搞迷糊掉。比如cold是多冷?controlled 是控到多少?room temperature是多少度?诸如此类,甚是困扰。 其实这些条件均来自美国药典USP,请见下面有关定义和中文解释。 1.freezer:一个温度控制在-25到-10℃的地方。 2.Referigerator:一个温度控制在2-8℃的地方 3.cold:任何温度不超过8℃的地方 4.cool: 任何温度在8到15℃的地方 5.room temperature:温度普遍和工作环境相当,也叫环境温度(Ambient temperature) 6. contolled room temperature: 温度维持在20到25℃之间。但这条美国药典有进一步的解释,Mean kinetic temperature not exceed 25°.Excurions between 15 and 30° that are experienced in pharmacies, hospitals, and warehouses, and during shipping are allowed.Provided the mean kinetic temperature does not exceed 25°,transient spikes up to 40° are permitted as long as they do not exceed 24h. Spike above 40° may be permitted only if the manufactures so
TOC美国药典
通常有两中方法来测量TOC。一种方法:确定TOC是用TC(测量得到的总碳量,即有机碳和非有机碳的总和)减去IC(测量得到的有机碳量): TOC=TC-IC。 另一种方法,是在开始测量各种碳之前,先清除掉样品中的IC(有机碳量)。然而,清除IC这一步也会除掉一部分有机分子,这部分有机分子被重新收集,氧化成CO2,定量为易除去的有机碳(POC)。样品中残留的有机物质也被氧化成CO2,定量为不易除去的有机碳(NPOC)。在这种方法中,TOC是POC和NPOC 的和: TOC=POC+NPOC。 在制药用水中,可以忽略不记POC的量。所以,在此方法中,NPOC相当于TOC。装置要求。使用一个在线或在非在线的实验室用校准的仪器测试。修正系统适应性,按下列描述定期进行。装置必须有特定的检测限度,含碳0.05mg/l(0.05ppm)或更低。 USP标准品--USP蔗糖标准品;USP1,4--苯醌标准品。 试剂水。使用总有机碳TOC不超过0.1mg/l的水。 [注意—可能对电导率有要求以保证方法的可靠性。] 玻璃器具准备。玻璃器具类的有机污染会导致较高的TOC值。所以要使用已经谨慎除去有机物质的玻璃器具和样品盛器。任何能够有效祛除有机物质的方法都可使用。用试剂水(TOC不超过0.1mg/l的水)最后冲洗玻璃器具。 标准溶液。精密称量USP蔗糖标准品,溶解于试剂水(TOC不超过0.1mg/l的水)中,获得浓度为每升含1.2mg蔗糖的溶液(既含碳0.50mg/l)。 供试溶液。[注意—在取样时要极其小心。水样在采集和移至实验设备的过程中都容易被污染。]采集供试水于一个密闭容器中,留有最小的顶空。尽快检查,减少来自容器和密封系统的污染。 系统适应性溶液。溶解精密称量的USP1,4--苯醌标准品于试剂水(TOC不超过0.1mg/l的水)中,获得一个浓度为0.75 mg/l的溶液(含碳0.50 mg/l)。 试剂水控制。使用一定数量的,在配制标准溶液和系统适应性溶液时用的TOC 水。 空白溶液。除了TOC水,还要配制适宜的空白溶液或其他溶液以建立基线或为校准调整用。进样适宜的空白溶液,调零仪器。 系统适应性。用装置检测,记录TOC水(r w),标准溶液(r s)。计算校正标准溶液值,也就是限度值,方法是用标准溶液的值减去TOC的值。理论限度,即含碳0.50 mg/l,等于校正过的标准溶液的值,r s- r w。系统适应性溶液(r ss). 计算校正后的系统适应性溶液值,方法是用系统适应性溶液的值减去TOC的值,r ss- r w。计算效率百分比: r ss- r w ×100 r s- r w 如果效率在理论值的85%~115%之间,系统适应。 步骤。检测供试溶液,记录r u。如果不大于r s- r w,符合实验。 本方法也适用在线仪器,仪器已经校准并具有可接受的系统适应性。安装位置和读数必须反映用水的水质。
中、美、英三国新版药典溶出度、释放度检查方法比较
中、美、英三国新版药典溶出度、释放度检查方法比较 许鸣镝胡琴 摘要:目的通过对中国药典、美国药典和英国药典中溶出度、释放度测定方法的比较,使广大药物分析工作者了解其异同,为新药开发及进出口检验服务。方法就其历史沿革,最新版所采用的仪器装置和结果判定等方面进行比较和讨论。结果三国药典收载的仪器装置各有异同,结果判定差异较大,应引起注意。结论如何能准确有效地监控药物释放过程,仍是有待深入研究和完善的课题。 关键词溶出度;释放度;中国药典;美国药典;英国药典 中图分类号:R921 文献标识码:E 文章编号:1001-2494(2000)07-0491-04 溶出度和释放度是指药物从片剂、胶囊剂和其它缓释、控释制剂中,在规定介质内,在一定条件下的溶出速度和溶出程度,是评价药物制剂质量的内在指标,是制剂质量控制的重要手段。 在药检工作中,经常要查阅中国药典、美国药典和英国药典。中国药典是我国药品的最高法典,而美国药典和英国药典由于历史悠久,技术先进又具有代表性,在世界各国有较大影响。有些国家没有药典,而以美国药典和英国药典为标准,在世界药品贸易中也常以其标准来要求。综观新版三国药典所收载的溶出度、释放度检查方法在很多方面趋向一致,但又在某些方面存在差别。下面仅就其历史沿革,最新版所采用的仪器装置和结果判定要求等方面进行比较和讨论。 1 历史沿革 1.1 中国药典 中国药典在1985年版引入溶出度检查法时,设定篮法、桨法及类似于流室法的装置等3种装置,1990年版仅保留了前2种装置,1995年版中增订了小杯法装置,并引入了释放度检查法,至2000年版又增加了测定透皮贴剂释放度所需的桨碟装置,方法发展很快。 1.2 美国药典 美国药典自1970年版(第18版)率先引入溶出度检查法,最初只设转篮法装置,且无图例。1975年版(第19版)增加了转篮法的图例,但与现在试验的篮法装置也不相同。1980年版(第20版)增设了桨法装置和改造后的崩解仪两种装置,未给出图例,也无统一的仪器配件尺寸规格。1985年版(第21版)起,规定了与现在溶出度试验所用篮法、桨法相同的装置,并引入释放度检查法,对缓释、肠溶制剂的溶出进行监控,装置与溶出度检查装置相同。1990年版(第22版)在上述规定的基础上,又增加了测定透皮贴剂的三种装置:桨碟法(paddle over disk),筒法(cylinder)及往复碟法(reciprocating disk)。至美国药典1995年版(第23版),用于溶出度、释放度测定的仪器增至7种,而最新版2000年版(第24版)在此基础上又进一步在设备上增加和完善,以适应更多剂型的要求。目前美国药典第24版已成为收载溶出度、释放度测定方法最多,规定最为详尽的药典。 1.3 英国药典 英国药典在1973年版中规定了地高辛片的溶出度和释放度检查,在1988年版引入溶出度检查法,设篮法、桨法两种装置,1993年版增加流室法装置,但未规定药物释放度检查法。在1998年版中,有关内容变化较大,按国际协调会(ICH)提出的要求,将试验片(个)数由5改为6,还增加了透皮贴剂的溶出度测定法(dissolution test for transdermal patches),并相应规定了3种装置。 由三国药典溶出度和释放度检查法的历史沿革可见,随着药品品种的增加,各国药典对药品的溶出度,释放度检查越来越重视,要求也越来越严格。最新版三国药典各论中收载的溶出度、释放度检查品种数量见表1。 表1
世界各国药典对药物残留溶剂测定法的比较研究
世界各国药典对药物残留溶剂测定法的比较研究 发表时间:2012-01-10T11:20:29.600Z 来源:《医药前沿》2011年第22期供稿作者:李明[导读] 为药物残留溶剂提供了不同药典测定的思路。 李明(江西省赣州卫生学校药学医技系江西赣州 341000)【中图分类号】R921.3/.7【文献标识码】A【文章编号】2095-1752(2011)22-0213-02 【摘要】目的比较世界各国药典对药物残留溶剂测定方法,为残留溶剂提供不同药典的测定思路。方法对ChP2010、USP34、BP2011、EP7.0、JP15收载的残留溶剂种类、限度、色谱检测方法和系统适用性要求,对照品及供试品的配制要求作了详细介绍。结论因为某一具体品种各生产企业引入的溶剂亦有不同而难于统一规定,国外药典通过混合对照品法对残留溶剂的测定控制较为严格,中国药典2010也逐步认识到残留溶剂测定的重要性。 【关键词】世界各国药典残留溶剂测定法药物中的残留溶剂系指在原料药或辅料的生产中,以及在制剂过程中使用或产生的,但在工艺过程中未能完全去除的有机溶剂。根据国际化学品安全性纲要,美国环境保护机构、世界卫生组织等一些国际组织的研究结果,很多有机溶剂对环境、人体都有一定的危害,因此,为保障药物的用药安全,控制产品质量,需要进行有机溶剂残留量的研究和控制。目前虽有陈立亚[1]和陈苏伟[2]等人发表了相关文章,但均未对各国药典中的残留溶剂测定法做系统的比较分析,本文通过对ChP2010、USP34、BP2011、EP7.0、JP15收载的残留溶剂种类、限度、色谱检测方法和系统适用性,对照品及供试品的配制要求作详细介绍。为药物残留溶剂提供了不同药典测定的思路。 1 各国药典收载的残留溶剂种类及限度目前ChP2010、USP34、BP2005、EP5.0、JP15 等残留溶剂的种类和限度的规定均参考人用药物注册技术要求国际协调会(International Conference on Harmonization of Technical Requirements for Registration of Pharmaceutical Use, ICH)颁布的指导原则。ICH于1996年11月6日颁布了残留溶剂测定指导原则征求意见稿,并对外公布,以便获取公众对指导原则的建议。该指导原则于1997年 7 月 17 日被ICH指导委员会采用,正式实施。 ICH 根据危害程度对残留溶剂进行了系统分类,“允许的日接触量”(permitted daily exposure ,PDE)的定义是指某一有机溶剂被允许摄入而不产生毒性的日平均最大剂量,单位为mg/天。依据毒性的不同,将69种残留溶剂分成了四类。(见表1)表 1 69种残留溶剂的分类 类别毒性 PDE(mg/天)第一类溶剂人体致癌物、疑为人体致癌物或环境危害物 0.1以下(1,1,1)三氯乙烷除外(15.0)第二类溶剂有非遗传致癌毒性或其他不可逆毒性、或其他严重的可逆毒性 0.5-50 第三类溶剂对人体低毒 50 以上 第四类溶剂尚无足够毒理学资料 PDE也一直是一个动态的修订过程,鉴于新的毒理学数据的获得,ICH 分别于2002年12月12日和10月28日修订了四氢呋喃(THF)和N-甲基吡咯烷酮(NMP)的PDE,将四氢呋喃(THF)由三类溶剂改为二类有机溶剂。ICH根据不同残留溶剂的的PDE值,制定了不同残留溶剂的限度。其中USP30版本之前对“残留溶剂”一直称为“有机挥发性杂质”(organic volatile impurities<467>,2008年7月1日美国药典统一改为了 “残留溶剂” (residual solvents <467>)。其中BP2011将环氧乙烷和二氧六环不再作为残留溶剂项下,而是另外作为一测定项单独列出。即各国药典收载的残留溶剂种类和限度是一致的,目前均遵守ICH 指导原则。 2 世界各国药典对残留溶剂色谱检测方法的比较世界各国药典均首选气相色谱法测定有机残留溶剂,但是具体在测定方法、色谱条件、供试品和对照品的制备、系统适用性方面有差别,下面分别予以比较。 2.1 ChP2010 的相关规定(表2)[3] 表2 ChP2010中残留溶剂的测定方法
中国、美国、欧洲药典比较
:徐涛学号:专业:中药生物技术学 《中国药典》、《美国药典》、《欧洲药典》比较 1、各国药典概况 1.1 历史沿革 《中国药典》 英文名称Pharmacopoeia of The People’s Republic of China;简称Ch .P。 1950年4月,成立了第一届中国药典编纂委员会,药典委员会分设名词、化学药、制剂、植物药、生物制品、动物药、药理、剂量8个小组,第一版《中国药典》于1953年由卫生部编印发行。1957年出版《中国药典》1953年增补本。1953年药典共收载药品531中,其中化学药215种,植物药与油脂类65种,动物药13种,抗生素2种,生物制品25种,各类制剂211种。 1965年1月26日卫生部颁布《中国药典》1963年版(第二版)发行通知和实施办法。本版药典收载药品1310种,分一、二部,各有凡例和有关的目录,一部收载中医常用的中药材446种和中药成方制剂197;二部收载化学药品667种。此外,一部记载药品的“功能主治”,二部增加了药品的“作用与用途”。 1979年10月4日卫生部颁布《中国药典》1977年版(第三版),自1980年1月1日起执行。本版药典共收载药品1925种,其中一部收载中草药材(包括少数民族药材)、中草药提取物、植物油脂以及单味药材制剂等882种,成方制剂(包括少数民族药成方)270种,共1152种;二部收载化学药品、生物制品等773种。 1985年9月出版《中国药典》1985年版(第四版),1986年4月1日起执行。本版收载药品1489种,其中一部收载中药材、植物油脂及单味制剂506种,成方制剂207种,共713种,二部收载化学药品、生物制品等776种。 1990年12月3日卫生部颁布《中国药典》1990年版(第五版),自1991年7月1日起执行。1990年版的第一、第二增补本先后于1992、1993年出版,英文版于1993年7月出版。本版共收载药品1751种,一部收载784种,其中中药材、植物油脂等509种,中药成方及单味制剂275种;二部收载化学制品、生物制品等967种。与1985年版药典收载品种相比,一部新增80种,二部新增213种,删去25种。药典二部项下规定的“作用与用途”和“用法与用量”分别改为“类别”和“剂量”。有关品种的红外光谱吸收图谱,收入《药品红外光谱集》另行出版,该版药典附录不在刊印。 1995年卫生部颁布《中国药典》1995版(第六版),自1996年4月1日起正式执行。本版药典收载药品2375种,一部收载920种,其中中药材、植物油脂522种,中药成方及单味制剂398种;二部收载1455种,包括化学药、抗生素、生化药、放射性药品、生物制品及辅料等。一部新增142种,二
USP《671》美国药典-包装容器——性能检测译文
《671》包装容器——性能检测 本章规定了用来包装的塑料容器及其组件功能性质上的标准(药品、生物制剂、营养补充剂和医疗器械),定义了保存、包装、存储和标签方面的凡例与要求。本文提供的试验用于确定塑料容器的透湿性和透光率。盛装胶囊和片剂的多单元容器章节适用于多单元容器。盛装胶囊和片剂的单位剂量容器章节适用于单位剂量容器。盛装胶囊和片剂的多单元容器(没有密封) 的章节适用于没有密封的聚乙烯和聚丙烯容器。盛装液体的多元和单元容器的章节适用于多元的和单元的容器。 一个容器想要提供避光保护或作为一个符合耐光要求的容器,由具有耐光的特殊性质的材料组成,包括任何涂层应用。一个无色透明或半透明的容器通过一个不透明的外壳包装变成耐光的(见凡例和要求 ),可免于对光的透射要求。在多单元容器和封盖与水泡的单位剂量容器由衬垫密封情况下,此处使用的术语“容器”指的是整个系统的组成。 盛装胶囊和片剂的多元容器 干燥剂——放置一些颗粒4—8目的无水氯化钙在一个浅的容器里,仔细剔除细粉,然后置于110°干燥,并放在干燥器中冷却。 试验过程——挑选12个类型和尺寸一致的容器,用不起毛的毛巾清洁密闭表面,并打开和关闭每个容器30次。坚决每次应用容器密闭一致。通过扭矩关闭螺旋盖容器,使气密性在附表规定的范围内。10个指定的测试容器添加干燥剂,如果容器容积大于等于20mL,每个填充13mm以内封闭;如果容器的容积小于20毫升,每个填充容器容量的三分之二。如果容器内部的深度超过63mm,惰性填料或垫片可以放置在底部来最小化容器和干燥剂的总重量;干燥剂层在这样一个容器中深度不低于5cm。添加干燥剂之后,立即按附表中规定的扭矩封闭螺旋帽容器。剩余的2个指定为对照容器,每个添加足够数量的玻璃珠,重量约等于每个测试容器的重量,并用附表中规定的扭矩封闭螺旋帽容器。记录各个容器的重量,如果容器的容积小于20毫升,精确到0.1毫克;如果容器容积为20毫升或以上但小于200毫升,精确到毫克;如果容器容积为200毫升及以上,精确到厘克(10毫克);在相对湿度75±3%和温度23±2°的环境下存储。[注意——浓度为35g/100mL的氯化钠溶液放在干燥器底部的渗透系统来维持指定湿度。其他的方法可以用来维护这些条件。] 336±1小时(14天)后,用同样的办法记录每个容器的重
各国药典介绍
各国药典介绍 欧洲药典(EP):https://www.wendangku.net/doc/0b17812532.html,/ 欧洲药典委员会1964年成立。1977年出版第一版《欧洲药典》。从1980年到1996年期间,每年将增修订的项目与新增品种出一本活页本,汇集为第二版《欧洲药典》各分册,未经修订的仍按照第一版执行。 1997年出版第三版《欧洲药典》合订本,并在随后的每一年出版一部增补本,由于欧洲一体化及国际间药品标准协调工作不断发展,增修订的内容显著增多。 时隔五年,第四版《欧洲药典》于2002年1月生效。最新版为第五版,即EP5.0,主册EP5.0于2004年夏天出版;增补版EP5.1和EP5.2于2005年出版。现已经出版到EP6.1。 美国药典(USP):https://www.wendangku.net/doc/0b17812532.html,/ U.S. Pharmacopeia / National Formulary《美国药典/国家处方集》(简称USP/NF)。由美国政府所属的美国药典委员会(The United States Pharmacopeial Convention)编辑出版。USP于1820年出第一版,1950年以后每5年出一次修订版,到2005年已出至第28版。NF1883年第一 版,1980年15版起并入USP,但仍分两部分,前面为USP,后面为NF。 美国药典是美国政府对药品质量标准和检定方法作出的技术规定,也是药品生产、使用、管理、检验的法律依据。NF收载了美国药典(USP)尚未收入的新药和新制剂。 美国药典正文药品名录分别按法定药名字母顺序排列,各药品条目大都列有药名、结构式、分子式、CAS登记号、成分和含量说明、包装和贮藏规格、鉴定方法、 干燥失重、炽灼残渣、检测方法等常规项目,正文之后还有对各种药品进行测试的方法和要求的通用章节及对各种药物的一般要求的通则。可根据书后所附的USP 和NF的联合索引查阅本书。 美国药典最新版为USP31-NF26。 英国药典(BP):https://www.wendangku.net/doc/0b17812532.html,/ 《英国药典》是英国药品委员会(British Pharmacopoeia Commission)的正式出版物,是英国制药标准的重要来源。英国药典不仅为读者提供了药用和成药配方标准以及公式配药标准,而且也向读者展示了许多 明确分类并可参照的欧洲药典专著。英国药典出版周期不定,最新的版本为2004年的第21版。 该药典由三卷本组成。其中两卷为英国药典、一卷为英国兽药典(兽医药品部分)。各条目均以药品名称字母顺序排列,内容包括药品性质、制法、血产品、免疫产品、电磁药品制法及外科材料等部分。英国药典书后附有全部内容
usp美国药典结构梳理
USP35-NF-30结构整理 vivi2010-10-02 USP总目录: 1 New Official Text修订文件 加快修订过程包括勘误表,临时修订声明(IRAS),修订公告。勘误表,临时修订声明,修订公告在USP网站上New Official Text部分刊出,勘误表,临时修订公告也会在PF上刊出2front matter前言 药典与处方集增补删减情况,审核人员,辅料收录情况 3凡例
药典, 1标题和修订 2 药典地位和法律认可 3标准复合性 4专论和通则 5 专论组成 6 检验规范和检验方法 7 测试结果 8 术语和定义 9 处方和配药 10 包装存储与标签 4通则 4.1章节列表 4.2一般检查和含量测定(章节编号小于1000)
检查和含量分析的一般要求 检查和含量分析的仪器, 微生物检查,生物检查和含量测定, 化学检查和含量测定, 物理检查和测定 4.3一般信息(章节号大于1000) 5食物补充剂通则 6试剂(试剂,指示剂,溶液等) 7参考表 性状描述和溶解性查询表(按字母顺序) 8食品补充剂各论(字母顺序) 9NF各论(辅料标准) 10 USP各论 11术语 附件:通则的章节中文目录(使用起来比较方便,直接找对应章节号即可)一、通用试验和检定 (1)试验和检定的总要求 1 注射剂 11 参比标准物 (2)试验和检定的装置 16 自动分析方法 21 测温仪 31 容量装置,如容量瓶、移液管、滴定管,各种规格的误差限度
41 砝码和天平 (3)微生物学试验 51 抗菌效力试验 55 生物指示剂:耐受性能试验 61 微生物限度试验 61 非灭菌制品的微生物检查:计数试验 62 非灭菌制品的特定菌检查,如大肠杆菌、金葡菌、沙门氏菌等 71 无菌试验 (4)生物学试验和检定 81 抗生素微生物检定 85 细菌内毒素试验 87 体外生物反应性试验:检查合成橡胶、塑料、高聚物对哺乳类细胞培养的影响 88 体内生物反应性试验:检查上述物质对小鼠、兔iv、ip或肌内植入的影响 91 泛酸钙检定 111 生物检定法的设计和分析 115 右泛醇检定 121 胰岛素检定 141 蛋白质——生物适应试验,用缺蛋白饲料大鼠,观察水解蛋白注射液和氨基酸混合物的作用 151 热原检查法 161 输血、输液器及类似医疗装置的内毒素、热原、无菌检查 171 维生素B12 活性检定 (5)化学试验和检定 A 鉴别试验 181 有机含氮碱的鉴别 191 一般鉴别试验 193 四环素类鉴别 197 分光光度法鉴别试验 201 薄层色谱鉴别试验 B 限量试验
各国药典储存条件汇总
各国药典储存条件汇总
————————————————————————————————作者: ————————————————————————————————日期:
药典储存条件的比较 2012-11-27 美国药典34 欧洲药典7.0 中国药典2010二部 冷冻储存-25℃~-10℃深冷低于-15℃ 冷处不超过8℃冷处2℃~10℃ 控制的冷处2℃~8℃,允许在0℃~15℃之 间 冰箱中储存2℃~8℃ 阴凉储存8℃~15℃阴凉储存8℃~15℃阴凉处不超过20℃ 凉暗处避光并不超过20℃室温工作区的一般温度 控制下的室温 储存20℃~25℃,允许在15℃~30℃ 之间 室温储存15℃~25℃常温10℃~30℃ 温暖30~40℃ 过热40℃以上 干燥储存控制室温下湿度不超过40% 见:药品GMP指南《质量控制实验室与物料系统》P387-388
药典加速、长期试验条件的比较 中国药典二部附录 试验名称试验条件备注1 备注2 加速试验(一般情况)温度40℃±2℃、相对湿度75%±5%所用设备应能控制温度±2℃,相对湿度 ±5%,并能对真实温度和湿度进行检测溶液剂、混悬剂、乳剂、注射液等含有水性介质的制剂可不要求相对湿度 加速试验(中间条件) 温度30℃±2℃、相对湿度 65%±5%在温度40℃±2℃、相对湿度75%± 5%加速6个月内不符合标准则采用该条 件 加速试验(温度敏感) 温度25℃±2℃、相对湿度60%± 10% 预计只能在冰箱中保存(4-8℃ 加速试验30℃±2℃、相对湿度 65%±5%乳剂、混悬剂、软膏剂、乳膏剂、糊剂、 凝胶剂、眼膏剂、栓剂、气雾剂、泡腾 剂及泡腾颗粒宜直接采用 加速试验40℃±2℃、相对湿度25%±5%包装在半透明容器中药物制剂,例如低 密度聚乙烯制备的输液袋、塑料安瓿、 眼用制剂容器等 长期试验(一般情况)温度在25℃±2℃、相对湿度 60%±1 0%或温度在30℃±2℃、相对湿度 6 5%±5% 南方、北方气候差异 长期试验(温度敏感)6℃±2℃ 长期试验温度在25℃±2℃、相对湿度 40%±5% 或温度在30℃±2℃、相对湿度3 5%±5% 包装在半透明容器中药物制剂选择由研究者决定
国内外药典贮藏条件下温度的规定
国内外药典贮藏条件下温度的规定 一、中国药典2010年版: 阴凉处:不超过20℃ 凉暗处:避光并不超过20℃ 冷处:2~10℃ 常温:10~30℃ 未规定贮藏温度的一般系指常温。 二、美国药典USP34: 冷冻(Freezer):-25~-10℃ 冷处(Cold):不超过8℃ 冷藏(A “refrigerator”is a cold place):2~8℃ 受控制的冷处(Controlled cold temperature):2~8℃,在贮存、运输及分配时允许在0~15℃。短时的可超过25℃,但应保证不超过24小时,除非有稳定性数据支持或生产商许可标识。 凉处(Cool):8~15℃ 室温(Room temperature):工作区温度 可控室温(Controlled room temperature):20~25℃,平均温度应不超过25℃。药房、医院、仓库允许在15~30℃。平均温度只要在范围内,短时的可超过40℃,但应保证不超过24小时。超过40℃应有生产商许可标识。 暖处(Warm):30~40℃
过热(Excessive heat):高于40℃ 干燥处(Dry place):在可控室温下,或在其他温度的等同气压下,平均相对湿度不超过40%。平均相对湿度可以直接测量,也可根据天气报告。测定可在一个季度、一年、或者药品的贮存期内,在不少于12次平行测定的基础上获得。平均相对湿度不超过40%,相对湿度偶尔过45%是允许的。 三、日本JP15: 标准温度(Standard temperature):20℃ 常温(Ordinary temperature):15~25℃ 室温(Room temperature):1~30℃ 凉处(A cold place):1~15℃ 微温(lukewarm):30~40℃ 四、欧洲药典EP7.0: 冷冻(In a deep-freeze):-15℃以下 冷藏(In a refrigerator):2~8℃ 冷处或凉处(Cold or cool):8~15℃ 室温(Room temperature):15~25℃
各国药典允许调整范围
各国药典允许调整范围 Adjusting Ph. Eur. Methods 欧洲药典调整范围 1. Mobile phase pH: ± 0.2 units ? pH of 7.6 can be adjusted from 7.4 – 7.8 流动相pH:0.2单位 例如:pH为7.6可以调整为7.4-7.8 2. Concentration of salts in buffer: ± 10 % ? 20 mM Potassium phosphate can be 18 – 22 mM, as long as proper pH is maintained as above 2.缓冲盐浓度:正负10% 20mM磷酸钾可以调整到18-22mM,pH的可调整范围如上。 3. Ratio of components in mobile phase: ± 30 % The amount(s) of the minor component(s) can be modified by ± 30 % relative or ±2 % absolute. However a change in any component cannot exceed ± 10 % absolute. ? 60:40 Acetonitrile/Water could be adjusted to ± 12 % water (= 30 % of 40), but this exceeds the ±10 % maximum absolute change. Therefore the amount of water can range from 30 % to 50 % in this case. 3.流动相组分的比率:正负30% 较少的组分能改变相对比率正负30%或绝对比率正负2%。但是任何组分的比率改变不能超过绝对比率的正负10%。 60:40乙腈:水可以调整为水的比率正负12%(30%乘以40),但是这超过了绝对比率正负10%。所以水的比率在这里可以在30%到50%的范围里调整。 4. Wavelength of UV-Visible Detector: no deviations permitted 4.紫外可见检测器的波长:不允许偏差 5. Column length: ± 70 % ? 150 x 4.6 mm col umn can be varied ± 105 mm in length 5.柱长:正负70% 150*4.6mm的柱子可以在长度上改变正负105mm。 6. Column inner diameter: ± 25 % ? 150 x 4.6 mm column can be varied ± 1.15 mm in diameter 6.柱内径:正负25% 150*4.6mm柱可以在直径上改变正负1.15mm
中国、美国、欧洲药典比较
姓名:徐涛学号:14211020462 专业:中药生物技术学 《中国药典》、《美国药典》、《欧洲药典》比较 1、各国药典概况 1.1 历史沿革 《中国药典》 英文名称Pharmacopoeia of The People’s Republic of China;简称Ch .P。 1950年4月,成立了第一届中国药典编纂委员会,药典委员会分设名词、 化学药、制剂、植物药、生物制品、动物药、药理、剂量8个小组,第一版 《中国药典》于1953年由卫生部编印发行。1957年出版《中国药典》1953年 增补本。1953年药典共收载药品531中,其中化学药215种,植物药与油脂类 65种,动物药13种,抗生素2种,生物制品25种,各类制剂211种。 1965年1月26日卫生部颁布《中国药典》1963年版(第二版)发行通知和实施办法。本版药典收载药品1310种,分一、二部,各有凡例和有关的目录,一部收载中医常用的中药材446种和中药成方制剂197;二部收载化学药品667种。此外,一部记载药品的“功能主治”,二部增加了药品的“作用与用途”。 1979年10月4日卫生部颁布《中国药典》1977年版(第三版),自1980 年1月1日起执行。本版药典共收载药品1925种,其中一部收载中草药材(包括少数民族药材)、中草药提取物、植物油脂以及单味药材制剂等882种,成 方制剂(包括少数民族药成方)270种,共1152种;二部收载化学药品、生物 制品等773种。 1985年9月出版《中国药典》1985年版(第四版),1986年4月1日起执行。本版收载药品1489种,其中一部收载中药材、植物油脂及单味制剂506种,成方制剂207种,共713种,二部收载化学药品、生物制品等776种。 1990年12月3日卫生部颁布《中国药典》1990年版(第五版),自1991 年7月1日起执行。1990年版的第一、第二增补本先后于1992、1993年出版,英文版于1993年7月出版。本版共收载药品1751种,一部收载784种,其中 中药材、植物油脂等509种,中药成方及单味制剂275种;二部收载化学制品、生物制品等967种。与1985年版药典收载品种相比,一部新增80种,二部新 增213种,删去25种。药典二部项下规定的“作用与用途”和“用法与用量” 分别改为“类别”和“剂量”。有关品种的红外光谱吸收图谱,收入《药品红 外光谱集》另行出版,该版药典附录内不在刊印。 1995年卫生部颁布《中国药典》1995版(第六版),自1996年4月1日起正式执行。本版药典收载药品2375种,一部收载920种,其中中药材、植物油脂522种,中药成方及单味制剂398种;二部收载1455种,包括化学药、抗生素、生化药、放射性药品、生物制品及辅料等。一部新增142种,二部新增品 种499种。二部药品外文名称改用英文名,取消拉丁名;中文名称只收载药品 法定通用名称,不再列副名。
15 API精烘包各国GMP法规要求汇总
非无菌API精烘包 各国GMP法规要求汇总 Pfizer COQA Sep2011 1 目录 ?非无菌药品 →中国98GMP标准的不足 →中国2010GMP标准实施 附录: 欧、美和WHO标准回顾 1.基本概念 2.标准介绍 3.发展趋势 2
3 非无菌API的生产环境 4 非无菌API的级别 ?对非无菌药品的环境监控来说,无官方的正式规定 ?但FDA还是希望看到非无菌API生产区有某种程度的监控?其关键点是对这类区域的级别不作规定,但生产区的设计应有适当的气流,并可能达到10万级的水平。指南中提到:应根据该区域的风险分析,来决定进行某种程度的环境监控。 ?比较典型的做法是监控空气微生物,取表面样,看清洁方法是否达到预期要求。这些区域没有规定级别,当然就不要求微粒的监控了。
5 欧美对非无菌API 的环境要求?欧美洁净级别是对无菌药品而言 ?无环境监测的强制规定,但GMP 检查时欧盟和FDA 希望看到某种程度的监测,如每月/季度一次?对非无菌API 生产环境洁区的要求,提到“如果可能,应按十万级设计并有适当的气流” ?总体认为:环境对非无菌生产的影响不大,现越来越多提倡进行风险评估 ?欧盟非无菌产品生产是否要求10万级? 欧洲药品管理局答复:不,欧盟GMP 中对非无菌产品不作规定 6 非无菌API 环境的其它信息?欧盟药品管理局没有30万级的提法。10万级也是对无菌药品的环境要求。?对非无菌产品及一般原料药而言,企业自己设HVAC 系统,静态测试,以确定设计标准。在生产过程中,洁净度(微粒)不需要作动态测试,只监控微生物指标。 ?更衣系统也不必完全与无菌药品相同。?征求了国内设计单位意见:建议非无菌药品可按10万级设计,以便有历史性衔接,且以前许多设计已这样做了,只考核静态,对动态指标与国际一致,不考核。 ?至于是否采用高效过滤器,可不作规定。
美国药典溶出介质缓冲液的配制
美国药典配制法 1在标准溶液配制标准指导下配制:0.2mol/L 盐酸溶液;0.2mol/L 氢氧化钠溶液 20.2mol/L邻苯二甲酸氢钾溶液:在水中溶解40.85g邻苯二甲酸氢钾,稀释制1000ml 3 0.2mol/L磷酸二氢钾溶液:在水中溶解27.22g磷酸二氢钾,稀释制1000ml 4 0.2mol/L硼酸氯化钾溶液:在水中溶解12.37g硼酸和14.91g氯化钾,稀释 至1000ml 5 0.2mol/L氯化钾溶液:在水中溶解14.91g氯化钾,稀释至1000ml 6 2N(当量浓度)的乙酸:在标准溶液配制标准指导下配制 标准缓冲液 盐酸缓冲液 将50ml氯化钾溶液置于200ml容量瓶中,加入一定量的盐酸溶液,用水定容至刻度 pH值 1.2 1.3 1.4 1.5 1.6 1.7 1.8 1.9 2.0 2.1 2.2 0.2mol/L 盐酸溶液(ml) 85.0 67.2 53.2 41.4 32.4 26.0 20.4 16.2 13.0 10.2 7.8 酸性邻苯二甲酸缓冲液 将50ml邻苯二甲酸氢钾溶液置于200ml容量瓶中,加入一定量的盐酸溶液,用水定容至刻度pH值 2.2 2.4 2.6 2.8 3.0 3.2 3.4 3.6 3.8 4.0 0.2mol/L 盐酸溶液(ml) 49.5 42.2 35.4 28.9 22.3 15.7 10.4 6.3 2.9 0.1 中性邻苯二甲酸缓冲液 将50ml邻苯二甲酸氢钾溶液置于200ml容量瓶中,加入一定量的氢氧化钠溶液,用水定容至刻度pH值 4.2 4.4 4.6 4.8 5.0 5.2 5.4 5.6 5.8
