无机化学实验第四版置换法测定镁的摩尔质量实验报告

实验名称:置换法测定镁的摩尔质量
实验日期:温度:气压:
一、实验目的
1.了解置换法测定镁的相对原子质量的原理和方法
2.掌握气态方程和分压定律的有关的计算
3.练习使用量气管和气压计
二、实验原理
1.在一定的温度T和压力P下,一定质量m的镁与足量的稀硫酸反应,可置换出一定体积y的氢气(含水蒸汽)Mg+H2SO4===MgSO4+H2
常压下的氢气可近似看作理想气体,根据气体状态方程和化学方程式,则有:
P H2V=n H2RT=(m/M)RT R为常数R=8.314 R的单位Pa*m3/mol*K T=(t+273)K
根据分压定律:P H2=P-P H2O,(我们所需的是氢气的压力,但是我们不能直接得到,所以我们通过大气的压力减去水蒸汽的压力便是我们想得到的氢气压力)
整理后可得:M=mRT/[(P-P H2O)]V
三、实验内容
1.用砂纸将镁条打光,清除掉表面氧化物膜,截取一段,在电子天平上准确称其质量。
2.装配好仪器,由漏斗注水至近于量气管刻度“0”的位置,上下移动漏斗以驱赶量气管与橡皮管内的气泡。
3.检查装置是否漏气,将各连接处的橡皮塞塞紧,把漏斗下移适当的距离固定,如果连气管内的液面只在开始时稍有下降,以后维持恒定,经3至5分钟不变,可判断装置不漏气。
4.将漏斗上移至原处,取下试管,用另外的漏斗向试管中注入c(H2SO4)=2mol/L溶液5mL(切勿使酸沾在试管内壁上)用一滴水将镁条沾在试管内壁上部,前确保镁条不与酸接触,将试管倾斜固定在铁架台上,塞紧橡皮塞,再一次检查装置是否漏气。(根据连通器的原理检查装置是否漏气)
5.将漏斗移至量气管近右侧,使两面处于同一水平面,几下量气管液面刻度。
6.将试管直立,使镁条落入酸中,而后将试管按原样固定,同时移动漏斗,是量气管与漏斗液面始终大体保持一致。
7.镁条反应完后,待试管冷至室温(约经十几分钟,也可用冷水在试管外冷却),将漏斗移至量气管近右侧,使两者处于同一水平,记下液面位置,稍等1至2分钟,再记下液面位置,若两次读数相等,即表示管内温度与室温一致。
8.记下实验时的室温和大气压力。
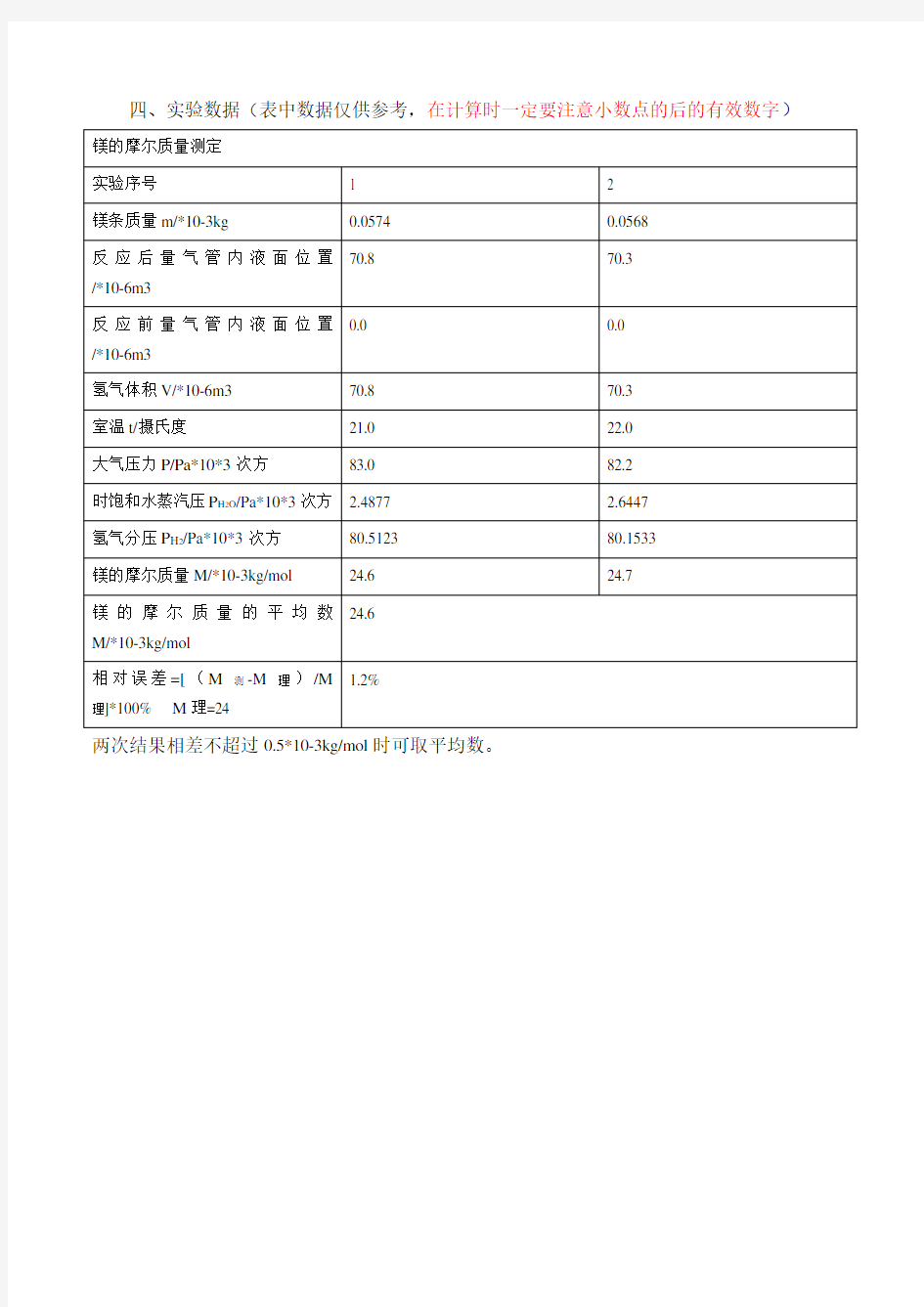
四、实验数据(表中数据仅供参考,在计算时一定要注意小数点的后的有效数字)镁的摩尔质量测定
实验序号 1 2
镁条质量m/*10-3kg 0.0574 0.0568
70.8 70.3
反应后量气管内液面位置
/*10-6m3
0.0 0.0
反应前量气管内液面位置
/*10-6m3
氢气体积V/*10-6m3 70.8 70.3
室温t/摄氏度21.0 22.0
大气压力P/Pa*10*3次方83.0 82.2
时饱和水蒸汽压P H2O/Pa*10*3次方 2.4877 2.6447
氢气分压P H2/Pa*10*3次方80.5123 80.1533
镁的摩尔质量M/*10-3kg/mol 24.6 24.7
24.6
镁的摩尔质量的平均数
M/*10-3kg/mol
1.2%
相对误差=[(M测-M理)/M
理]*100% M理=24
两次结果相差不超过0.5*10-3kg/mol时可取平均数。
单缝衍射实验实验报告
单缝衍射实验 一、实验目的 1.观察单缝衍射现象,了解其特点。 2.测量单缝衍射时的相对光强分布。 3.利用光强分布图形计算单缝宽度。 二、实验仪器 He-Ne激光器、衍射狭缝、光具座、白屏、光电探头、光功率计。 三、实验原理 波长为λ的单色平行光垂直照射到单缝上,在接收屏上,将得到单缝衍射图样,即一组平行于狭缝的明暗相间条纹。单缝衍射图样的暗纹中心满足条件: (1) 式中,x为暗纹中心在接收屏上的x轴坐标,f为单缝到接收屏的距离;a为单缝的宽度,k为暗纹级数。在±1级暗纹间为中央明条纹。中间明条纹最亮,其宽度约为其他明纹宽度的两倍。 实验装置示意图如图1所示。 图1 实验装置示意图 光电探头(即硅光电池探测器)是光电转换元件。当光照射到光电探头表面时在光电探头的上下两表面产生电势差ΔU,ΔU的大小与入射光强成线性关系。光电探头与光电流放大器连接形成回路,回路中电流的大小与ΔU成正比。因此,通过电流的大小就可以反映出入射到光电探头的光强大小。 四、实验内容 1.观察单缝衍射的衍射图形;
2.测定单缝衍射的光强分布; 3.利用光强分布图形计算单缝宽度。 五、数据处理 ★(1)原始测量数据 将光电探头接收口移动到超过衍射图样一侧的第3级暗纹处,记录此处的位置读数X(此处的位置读数定义为0.000)及光功率计的读数P。转动鼓轮,每转半圈(即光电探头每移动0.5mm),记录光功率测试仪读数,直到光电探头移动到超过另一侧第3级衍射暗纹处为止。实验数据记录如下: 将表格数据由matlab拟合曲线如下:
★ (2)根据记录的数据,计算单缝的宽度。 衍射狭缝在光具座上的位置 L1=21.20cm. 光电探测头测量底架座 L2=92.00cm. 千分尺测得狭缝宽度 d’=0.091mm. 光电探头接收口到测量座底座的距离△f=6.00cm. 则单缝到光电探头接收口距离为f= L2 - L1+△f=92.00cm21.20cm+6.00cm=76.80cm. 由拟合曲线可读得下表各级暗纹距离: 各级暗纹±1级暗纹±2级暗纹±3级暗纹 距离/mm 10.500 21.500 31.200 单缝宽度/mm 0.093 0.090 0.093 单缝宽度计算过程: 因为λ=632.8nm.由d =2kfλ/△Xi,得 d1=(2*1*768*632.8*10^-6)/10.500 mm=0.093mm. d2=(2*2*768*632.8*10^-6)/21.500 mm=0.090mm.
物质的摩尔质量
(二)物质的量 1. 物质的量:表示物质含有微粒集体多少的物理量。 2. 符号:n 单位:mol 3. 物质的量的基准:以g 12C 12所含的碳原子数(即阿伏加德罗常数)作为物质的量的 基准。 阿伏加德罗常数? ???-1231002.6mol N A ::近似值精确值 即物质约含有231002.6?个微粒,它的物质的量就为mol 1。 4. 说明 (1)物质的量这一物理量只用于微观,不适于宏观物质的描述,如不能说成“mol 1米” (2)使用时必须指明物质的种类,即用化学式表示。 (3)物质的量相同的任何物质所含有微粒数也相同。 5. 粒子数与其物质的量的关系:A N N n = 6. 化学计量数(γ)和物质的量之间的关系: 点燃=== +222O H O H 22 化学计量数之比 2 : 1 : 2 粒子数之比 2 : 1 : 2 物质的量之比 2 : 1 : 2 (三)摩尔质量 1. 定义:单位物质的量的物质所具有的质量。 2. 符号:M 单位:mol g /或mol kg / 3. 物质的量、物质的质量、摩尔质量的关系 n m M = n M m ?= M m n = 4. 粒子的摩尔质量的数值 m o l 1任何原子以克为单位时,在数值上等于该种原子的相对原子质量。 m o l 1任何分子以克为单位时,在数值上等于该种分子的相对分子质量。 m o l 1任何离子以克为单位时,在数值上等于形成该种离子的原子的相对原子质量。 【典型例题】 [例1] 下列几种说法是否正确? A. 摩尔是基本物理量之一 B. 某物质含有23 1002.6?个微粒,这种物质就是mol 1。 C. mol 1氢 D. 气体体积越大,所含气体的物质的量就越多,相应的分子数目也越多。
《物质的量单位摩尔》教案
第二节化学计量在实验中的应用 教学重点与难点 教学重点: ①物质的量及其单位、阿伏加德罗常数;②摩尔质量概念和有关摩尔质量的计算;③ 物质的量浓度的概念及有关计算;④一定物质的量浓度的溶液的配制方法。 教学难点: ①物质的量概念的教学;②摩尔质量、气体摩尔体积概念的建立;③物质的量浓度的 概念及有关计算。 教学方式 本节课属于概念教学课,根据概念教学的一般原则,主要运用讲授方式、形象化的启发式教学法、类比逻辑方法,帮助学生理解概念,掌握概念,并灵活应用概念。对于概念课的教授,因为抽象、理解难度大,学生相对会缺乏学习兴趣,所以应该激发学生的学习积极性,在概念引入时强调它在化学中的必要性,激发学生学习的紧迫感。另外,在教学中一定要注意教学过程的逻辑性,用思维的逻辑性吸引学生的注意力。 学生在初中学习了原子、分子、电子等微观粒子,学习了化学方程式的意义和常用的物理量及其对应的单位,这是学习本节课的知识基础,但是本节课的概念多,理解难度大,而且学生还没有适应高中的化学学习,所以教师应注意从学生认识基础出发,加强直观性教学,采用设问、类比启发、重点讲解并辅以讨论的方法,引导学生去联想,运用迁移规律,使学生在轻松的环境中掌握新知识。在实验课中,要注重让学生自己去尝试并探讨,在过程中感受和学习。 第一课时:物质的量的单位——摩尔 引入 教师:买大米时我们一般论斤买而论“粒”就不方便,一斤就是许多“粒”的集体;买纸可以论张买,但是买多了论“令”就比较方便,“令”就是500张的集体,买矿泉水我们可以论瓶买,但买多的也可以论箱买,一箱就是24瓶的集体等等。那么化学中的粒子论个可能数不清,我们能否引入一个新的物理量解决这个问题呢 我们在初中已经知道分子、原子、离子等我们肉眼看不见的微观粒子,它们可以构成我们看得见的、客观存在的,具有一定质量的宏观物质。这说明,在我们肉眼看不见的微观粒子与看得见的宏观物质之间必定存在某种联系。例如我们已经知道反应: 2H2+ O2点燃2H2O 微观角度:2个氢分子1个氧分子2个水分子 宏观角度: 4 g 32 g 36 g
常见元素的摩尔质量表
常见元素的摩尔质量表 112-118号元素数据未被IUPAC确定。 1 氢 H 1.007 94(7 2 氦 He 4.002 602(2 3 锂 Li 6.941(2 4 铍 Be 9.012 182(3 5 硼 B 10.811(7 6 碳 C 12.017(8 7 氮 N 14.006 7(2 8 氧 O 15.999 4(3 9 氟 F 18.998 403 2(5 10 氖 Ne 20.179 7(6 11 钠 Na 22.989 769 28(2 12 镁 Mg 24.305 0(6 13 铝 Al 26.981 538 6(8 14 硅 Si 28.085 5(3 15 磷 P 30.973 762(2 16 硫 S 32.065(5 17 氯 Cl 35.453(2 18 氩 Ar 39.948(1 19 钾 K 39.098 3(1 20 钙 Ca 40.078(4 21 钪 Sc 44.955 912(6 22 钛 Ti 47.867(1 23 钒 V 50.941 5(1 24 铬 Cr 51.996 1(6 25 锰 Mn 54.938 045(5 26 铁 Fe 55.845(2 27 钴 Co 58.933 195(5 28 镍 Ni 58.693 4(2 29 铜 Cu 63.546(3 30 锌 Zn 65.409(4 31 镓 Ga 69.723(1
33 砷 As 74.921 60(2 34 硒 Se 78.96(3 35 溴 Br 79.904(1 36 氪 Kr 83.798(2 37 铷 Rb 85.467 8(3 38 锶 Sr 87.62(1 39 钇 Y 88.905 85(2 40 锆 Zr 91.224(2) 41 铌 Nb 92.906 38(2 42 钼 Mo 95.94(2 43 锝 Tc [97.9072] 44 钌 Ru 101.07(2 45 铑 Rh 102.905 50(2 46 钯 Pd 106.42(1 47 银 Ag 107.868 2(2 48 镉 Cd 112.411(8 49 铟 In 114.818(3 50 锡 Sn 118.710(7 51 锑 Sb 121.760(1 52 碲 Te 127.60(3 53 碘 I 126.904 47(3 54 氙 Xe 131.293(6 55 铯 Cs 132.905 451 9(2 56 钡 Ba 137.327(7 57 镧 La 138.905 47(7 58 铈 Ce 140.116(1 59 镨 Pr 140.907 65(2 60 钕 Nd 144.242(3 61 钷 Pm [145] 62 钐 Sm 150.36(2 63 铕 Eu 151.964(1 64 钆 Gd 157.25(3 65 铽 Tb 158.925 35(2 66 镝 Dy 162.500(1 67 钬 Ho 164.930 32(2 68 铒 Er 167.259(3 69 铥 Tm 168.934 21(2
迈克尔逊干涉仪实验报告
实验目的: 1)学会使用迈克尔逊干涉仪 2)观察等倾、等厚和非定域干涉现象 3)测量氦氖激光的波长和钠光双线的波长差。 实验仪器: 氦氖激光光源、钠光灯、迈克尔逊干涉仪、毛玻璃屏 实验原理: 1:迈克尔逊干涉仪的原理: 迈克尔逊干涉仪的光路图如图所示,光源S 出发的光经过称。45放置的背面镀银的半透玻璃板1P 被分成互相垂直的强度几乎相等的两束光,光 路1通过1M 镜反射并再次通过1P 照射在观察平 面E 上,光路2通过厚度、折射率与1P 相同的玻 璃板2P 后由2M 镜反射再次通过2P 并由1P 背面 的反射层反射照射在观察平面E 上。图中平行于1M 的'2M 是2M 经1P 反射所成的虚像,即1P 到2M 与1P 到'2M 的光程距离相等,故从1P 到2M 的光路可用1P 到'2M 等价替代。这样可以认为1M 与'2M 之间形成了一个空气间隙,这个空气间隙的厚度可以通过移动1M 完成,空气间隙的夹角可以通过改变1M 镜或2M 镜的角度实现。当1M 与' 2M 平行时可以在观察平面E 处观察到等倾干涉现象,当1M 与'2M 有一定的夹角时可以在观察平面E 处观察到等厚干涉现象。 2:激光器激光波长测量原理: 由等倾干涉条纹的特点,当θ =0 时的光程差δ 最大,即圆心所对应的干
涉级别最高。转动手轮移动 M1,当 d 增加时,相当 于增大了和 k 相应的θ 角 ,可以看到圆 环一个个从中心“冒出” ;若 d 减小时,圆环逐渐 缩小,最后“淹没”在中心处。 每“冒”出或“缩”进一个干涉环,相应的光程差改变了一个波长,也就是 M 与M ’之间距离 变化了半个波长。 若将 M 与 M ’之间距离改变了△d 时,观察到 N 个干涉环变化,则△d =N 由此可测单色光的波长。 3:钠光双线波长差的测定: 在使用迈克尔逊干涉仪观察低压钠黄灯双线的等倾干涉条纹时,可以看到随着动镜1M 的移动,条纹本身出现了由清晰到模糊再到清晰的周期性变化,即反衬度从最大到最小再到最大的周期性变化,利用这一特性,可测量钠光双线波长差,对于等倾干涉而言,波长差的计算公式为: 实验内容与数据处理: (1)观察非定域干涉条纹 1)通过粗调手轮打开激光光源,调节激光器使其光束大致垂直于平面反光镜2M 入射,取掉投影屏E ,可以看到两排激光点 2)粗调手轮移动1M 镜的位置,使得通过分光板分开的两路光光程大致相等 3)调节1M 、2M 镜后面的两个旋钮,使两排激光点重合为一排,并使两个最亮的光点重合在一起。此时再放上投影屏E ,就可以看到干涉条纹。 4)仔细调节1M 、2M 镜后面的两个旋钮,使1M 与' 2M 平行,这时在屏上可以看到同心圆条纹,这些条纹为非定域条纹。 5)转动微调手轮,观察干涉条纹的形状、疏密及中心“吞”、“吐”条纹随光程差改变的变化情况。
常见元素的摩尔质量表
常见元素的摩尔质量表注:期前方序列号不为原子序数、 1、氢 H 1 2、氦 He 4 3、锂 Li 7 4、铍 Be 9 5、硼 B 11 6、碳 C 12 7、氮 N 14 8、氧 O 16 9、氟 F 19 10、氖 Ne 20 11、钠 Na 23 12、镁 Mg 24 13、铝 Al 27 14、硅 Si 28 15、磷 P 31 16、硫 S 32 17、氯 Cl 35.5 18、氩 Ar 40 19、钾 K 39 21、钙 Ca 40 22、铬 Cr 52 23、锰 Mn 55 24、铁 Fe 56 25、镍 Ni 58.69 26、铜 Cu 64
27、锌 Zn 65 28、镓 Ga 69.723(1 29、砷 As 75 30、硒 Se 79 31、溴 Br 80 32、银 Ag 108 33、镉 Cd 112.411(8 34、铟 In 114.818(3 35、锡 Sn 118.710(7 36、锑 Sb 121.760(1 37、碘 I 127 38、铯 Cs 133 39、钡 Ba 137.327(7 40、铂 Pt 195.084(9 41、金 Au 196.966 569(4 42、汞 Hg 200.59(2 43、镭 Re 226 _ 平均摩尔质量 М(平~量)=m总/n总 M=PVm (P代表气体密度) 例如:CO2 H2 CO 的混合气体 , 同温同压求平均摩尔质量. _ M=m总/n总=M1*a%+M2*b%+M3*c%+~~~~~ 这是阿伏伽德罗定律的变形 平均摩尔质量 =混合物中各组分的摩尔质量×该组分的物质的量分数(若是气体组分可以是体积分数)
物质的量教学案
02 物质的量 【学习目标】知道摩尔是物质的量的基本单位,初步学会物质的量、摩尔质量、质量之间的简单计算,体会定量研究的方法对研究和学习化学的重要作用 【学习重点】物质的量及其单位和有关物质的量的简单计算 【学习难点】对物质的量及其单位的理解 基本物理量长度质量时间物质的量电流强度热力学温度发光强度单位米千克秒摩尔安培开尔文坎德拉 符号m kg s mol A K cd 在化学反应中的微粒质量很小但数目很大,如何把一定数目的微观粒子与可称量的宏观物质联系起来呢?所以引进一个新的基本物理量——物质的量。 一、物质的量 1、物质的量:是国际单位制中的一个___________,表示 符号: 2、物质的量的单位:______,简称为_______,符号:_______(例:n(H2O)=1mol) 1mol 某种微粒集合体中所含的微粒数与相同。使用物质的量的注意点: 3、阿伏加德罗常数: (1)_______________________________称为阿伏加德罗常数 (2)阿伏加德罗常数的符号及单位______________________ (3)阿伏加德罗常数的近似值______________________ 【例1】下列说法中,正确的是() A.摩尔是物质的量的单位,是七个国际基本物理量之一。 B.阿伏加德罗常数是12g碳中所含的碳原子数 C.物质的量就是物质的质量D.物质的量就是物质所含微粒数目的多少E.阿伏加德罗常数就是6.02×1023mol-1 F.摩尔是表示物质粒子多少的物理量G.物质的量适用于计量分子、原子、离子等粒子 【归纳】 4、物质的量(n)与阿伏加德罗常数(N A)、微粒数(N)之间的关系:
迈克尔逊干涉仪实验报告
迈克尔逊干涉仪实验报告 Final approval draft on November 22, 2020
迈克尔逊干涉仪(实验报告) 一、实验目的 1、掌握迈克尔逊干涉仪的调节方法并观察各种干涉图样。 2、区别等倾干涉、等厚干涉和非定域干涉,测定 He-Ne 激光波长 二、实验仪器 迈克尔逊干涉仪、 He-Ne 激光器及光源、小孔光阑、扩束镜(短焦距会聚镜)、毛玻璃屏等。 (图一) (图二) 三、实验原理 ①用 He-Ne 激光器做光源,使激光通过扩束镜会聚后发散,此时就得到了一个相关性很好的点光源,射到分光板P1和 P2上后就将光分成了两束分别射到 M1 和 M2 上,反射后通过 P1 、 P2 就可以得到两束相关光,此时就会产生干涉条纹。 ②产生干涉条纹的条件,如图 2 所示, B 、 C 是两个相干点光源,则到 A 点的光程差δ =AB-AC=BCcosi , 若在 A 点出产生了亮条纹,则δ =2dcosi=k λ (k 为亮条纹的级数 ) ,因为 i 和 k 均为不可测的量,所以取其差值,即λ =2 Δ d/ Δ k 。 四、实验步骤 1、打开激光电源,先不要放扩束镜,让激光照到分光镜 P1 上,并调节激光的反射光照射到激光筒上。 2、调节 M2 的位置使屏上两排光中最亮的两个光点重回,并调至其闪烁。 3、将扩束镜放于激光前,调节扩束镜的高度和偏角,使光能照在 P1分光镜上,看显示屏上有没有产生同心圆的干涉条纹图案。没有的话重复 2 、 3 步骤,直到产生同心圆的干涉条纹图案。 4、微调 M2是干涉图案处于显示屏的中间。 5、转动微量读数鼓轮,使 M1 移动,可以看到中心条纹冒出或缩进,若看不到此现象,先转动可度轮,再转动微量读数鼓轮。记下当前位置的读数 d0 ,转动微量读数鼓轮,看到中心条纹冒出或缩进 30 次则记一次数据,共记录10 次数据即 d0、 d1 (9) 6、关闭激光电源,整理仪器,处理数据。 五、实验数据处理 数据记录: 数据处理: Δd0=d5-d0= Δd1=d6-d1= Δd2=d7-d2= Δd3=d8-d3= Δd4=d9-d4= Δd(平均)=(Δd0+Δd1+Δd2+Δd3+Δd4)/5 =
摩尔质量教学设计
摩尔质量教学设计 知识与技能: 1.使学生了解摩尔质量的概念,了解摩尔质量与相对原子质量、相对分子质量之间的关系。 2.使学生了解物质的量、摩尔质量与物质的质量之间的关系。过程与方法: 1.通过对数据的分析比较,培养学生的分析问题、科学处理数据的能力。 2.,培养学生的计算能力,并通过计算帮助学生更好地理解概念和运用、巩固概念。 3.培养学生逻辑推理、抽象概括的能力。 情感、态度与价值观: 1.使学生认识到微观和宏观的相互转化是研究化学的科学方法之一,培养学生尊重科学的思想。 2.通过学生的置疑、解疑,激发学生对问题的探究兴趣及探究能力。 3.通过计算,强调解题规范,养成良好的计算习惯。 教学重点:摩尔质量的概念。 教学难点:摩尔质量的概念。 [教学过程] [导入新课]什么是物质的量?什么是摩尔?它们的使用范围是什么 [学生]物质的量是表示物质所含粒子多少的物理量,摩尔是物质的量的单位。每摩尔物质都含有阿伏加德罗常数个粒子,阿伏加德罗常数的近似值为6.02×1023mol-1。物质的量和摩尔都只适用于微观粒子,不能用用于宏观物体。 [讲述]既然物质的量是联系微观粒子和宏观物体的桥梁,那么,物质的量是如何把微观粒子与宏观质量、体积联系起来的呢?这节课我们就来研究物质的量与质量之间的关系。 [推进新课]分析书中表格l一3-1中列出的1mol 物质的质量与其相对原子质量或相对分子质量的关系。 [学生]1mol原子的质量在数值上等于它的相对原子质量。1mol分子的质量在数值上等于它的相对分子质量。 [提问]那么,对于粒子中的离子来讲,又将怎样呢? [学生]对于离子来说,由于电子的质量很小,当原子得到或失去电子变成离子时,电子的质量可略去不计,因此,1mol离子的质量在数值上等于该离子的式量。
物质的量单位——摩尔优质课教案
教学设 物质的量的单位—摩尔 姓名:王雪 §1.2.1物质的量的单位———摩尔 执教人:王雪 【教学目标】 1、知识与技能目标: (1)使学生领会物质的量、摩尔、阿伏伽德罗常数的基本含义。 (2)使学生理解物质的量、阿伏伽德罗常数之间的相互关系,学会用物质的量来计量物质。 2、过程与方法目标: (1)通过引导学生对自己熟悉问题的分析,让他们学会怎样从中提炼总结出解决问题的科学方法。 (2)通过模拟科学家解决实际问题的探究活动,让学生感受科学家在面对实际问题时,如何分析、联想、类比、迁移、概括和总结,如何建立数学模型,培养他们解决实际问题的能力。 3、情感态度与价值观目的: 通过模拟科学家解决实际问题的探究活动,激发学生探索未知世界的兴趣,让他们享受到探究未知世界的乐趣。【教学重点】物质的量及其单位,摩尔质量的概念和有关摩尔质量的计算 【教学难点】物质的量及其单位 【教学方法】启发式教学法、小组讨论法 【教具】多媒体,投影仪 【教学过程】 [引言]生活中买米,建筑中买沙子,为什么不用“粒”来计量呢? 用“粒”计量,数目太大,也很不方便。 把很多米或沙子看成一个集体,一袋米,一吨沙子,这样算起来就方便多了。 同学们。我这里有一杯水.请问,我们可以通过哪些物理量来描述有多少水呢?请同学们从多角度来分析 [生]展开分组讨论 质量、体积,水分子数...... 引导学生回答,水的质量可以用天平称量,水的体积可以用量筒量取。那么水分子的个数呢?可以直接用仪器测量吗?如果不能直接测量,那么我们怎么才能知道这杯水中含有多少个水分子呢?能不能像数铅笔一样一个一个的数呢? [生]不能,太多了。。。。。。 太小了。。。。。。 【投影】一滴水中的分子个数
塞曼效应实验报告
近代物理实验报告 塞曼效应实验 学院 班级 姓名 学号 时间 2014年3月16日
塞曼效应实验实验报告 【摘要】: 本实验通过塞曼效应仪与一些观察装置观察汞(Hg)546.1nm谱线(3S1→3P2跃迁)的塞曼分裂,从理论上解释、分析实验现象,而后给出横效应塞满分裂线的波数增量,最后得出荷 质比。 【关键词】:塞曼效应、汞546.1nm、横效应、塞满分裂线、荷质比 【引言】: 塞曼效应是原子的光谱线在外磁场中出现分裂的现象,是1896年由荷兰物理学家塞曼发现的。首先他发现,原子光谱线在外磁场发生了分裂;随后洛仑兹在理论上解释了谱线分裂成 3条的原因,这种现象称为“塞曼效应”。在后来进一步研究发现,很多原子的光谱在磁场中 的分裂情况有别于前面的分裂情况,更为复杂,称为反常塞曼效应。 塞曼效应的发现使人们对物质光谱、原子、分子有更多了解,塞曼效应证实了原子磁矩的 空间量子化,为研究原子结构提供了重要途径,被认为是19世纪末20世纪初物理学最重要的发现之一。利用塞曼效应可以测量电子的荷质比。在天体物理中,塞曼效应可以用来测量天体 的磁场。本实验采取Fabry-Perot(以下简称F-P)标准具观察Hg的546.1nm谱线的塞曼效应,同时利用塞满效应测量电子的荷质比。 【正文】: 一、塞曼分裂谱线与原谱线关系 1、磁矩在外磁场中受到的作用 (1)原子总磁矩在外磁场中受到力矩的作用: 其效果是磁矩绕磁场方向旋进,也就是总角动量(P J)绕磁场方向旋进。 (2)磁矩在外磁场中的磁能:
由于或在磁场中的取向量子化,所以其在磁场方向分量也量子化: ∴原子受磁场作用而旋进引起的附加能量 M为磁量子数 g为朗道因子,表征原子总磁矩和总角动量的关系,g随耦合类型不同(LS耦合和jj耦合)有两种解法。在LS耦合下: 其中: L为总轨道角动量量子数 S为总自旋角动量量子数 J为总角动量量子数 M只能取J,J-1,J-2 …… -J(共2J+1)个值,即ΔE有(2J+1)个可能值。 无外磁场时的一个能级,在外磁场作用下将分裂成(2J+1)个能级,其分裂的能级是等间隔的,且能级间隔 2、塞曼分裂谱线与原谱线关系: (1) 基本出发点:
摩尔质量
第2课时 教学设计 三维目标 知识与技能 1.使学生了解摩尔质量的概念。了解摩尔质量与相对原子质量、相对分子质量之间的关系。 2.使学生了解物质的量、摩尔质量、物质的质量之间的关系,掌握有关概念的计算。 3.进一步加深理解巩固物质的量和摩尔的概念。 过程与方法 1.培养学生的逻辑推理、抽象概括的能力。 2.培养学生的计算能力,并通过计算帮助学生更好地理解概念和运用、巩固概念。 情感、态度与价值观 1.使学生认识到微观和宏观的相互转化是研究化学的科学方法之一。培养学生尊重科学的思想。 2.强调解题规范化,单位使用准确,养成良好的学习习惯。 教学重点 摩尔质量的概念和相关计算 教学难点 摩尔质量与相对原子质量、相对分子质量之间的关系 教具准备 多媒体课件、投影仪 教学过程 引入新课 师:什么是物质的量?什么是摩尔?它们的使用范围是什么? 生:物质的量是表示物质所含粒子多少的物理量,摩尔是物质的量的单位。每摩尔物质都含有阿伏加德罗常数个粒子,阿伏加德罗常数的近似值为6.02×1023 mol-1。物质的量和摩尔都只适用于表示微观粒子,不能用于表示宏观物体。在使用物质的量时应该用化学式指明粒子的种类。 师:既然物质的量是联系微观粒子和宏观物质的桥梁,那么如何通过物质的量求出物质的质量呢?也就是说1 mol物质的质量到底有多大呢?我们先填写下面的表格,看是否可以从这些数据中得出有用的结论。 [多媒体展示] [多媒体展示] H2O的相对分子质量是18,1 mol水含6.02×1023个水分子,质量是18 g,Al的相对原子质量为27,1 mol铝含6.02×1023个铝原子,质量是27 g。C的相对原子质量为12,1 mol
迈克尔逊干涉仪实验报告
迈克尔逊干涉仪实验报告 一、实验题目:迈克尔逊干涉仪 二、实验目的: 1. 了解迈克尔逊干涉仪的结构、原理和调节方法; 2. 观察等倾干涉、等厚干涉现象; 3. 利用迈克尔逊干涉仪测量He-Ne激光器的波长; 三、实验仪器: 迈克尔逊干涉仪、He-Ne激光器、扩束镜、观察屏、小孔光阑四、实验原理(原理图、公式推导和文字说明): 在图M 2′是镜子M 2 经A面反射所成的虚像。调整好的迈克尔逊干涉仪,在 标准状态下M 1、M 2 ′互相平行,设其间距为d.。用凸透镜会聚后的点光源S是 一个很强的单色光源,其光线经M 1、M 2 反射后的光束等效于两个虚光源S 1 、S 2 ′ 发出的相干光束,而S 1、S 2 ′的间距为M 1 、M 2 ′的间距的两倍,即2d。虚光源 S 1、S 2 ′发出的球面波将在它们相遇的空间处处相干,呈现非定域干涉现象,其 干涉花纹在空间不同的位置将可能是圆形环纹、椭圆形环纹或弧形的干涉条纹。 通常将观察屏F安放在垂直于S 1、S 2 ′的连线方位,屏至S 2 ′的距离为R,屏上 干涉花纹为一组同心的圆环,圆心为O。 设S 1、S 2 ′至观察屏上一点P的光程差为δ,则 )1 /) (4 1 ( ) 2 ( 2 2 2 2 2 2 2 2 2 - + + + ? + = + - + + = r R d Rd r R r R r d R δ (1) 一般情况下d R>>,则利用二项式定理并忽略d的高次项,于是有
??? ? ??+++=? ??? ??+-++?+=)(12)(816)(2)(4222 22222222222 2 r R R dr r R dR r R d R r R d Rd r R δ (2) 所以 )sin 1(cos 22θθδR d d + = (3) 由式(3)可知: 1. 0=θ,此时光程差最大,d 2=δ,即圆心所对应的干涉级最高。旋转微调鼓轮使M 1移动,若使d 增加时,可以看到圆环一个个地从中心冒出,而后往外扩张;若使d 减小时,圆环逐渐收缩,最后消失在中心处。每“冒出”(或“消失”)一个圆环,相当于S 1、S 2′的距离变化了一个波长λ大小。如若“冒出”(或“消失”)的圆环数目为N ,则相应的M 1镜将移动Δd ,显然: N d /2?=λ (4) 从仪器上读出Δd 并数出相应的N ,光波波长即能通过式(4)计算出来。 2. 对于较大的d 值,光程差δ每改变一个波长所需的θ的改变量将减小,即两相邻的环纹之间的间隔变小,所以,增大d 时,干涉环纹将变密变细。 五、实验步骤 六、实验数据处理(整理表格、计算过程、结论、误差分析): m m 105-5?=?仪 N=30
物质的量教案(第一课时)
化学计量在实验中的应用(第1课时) 一、教学目标 【知识目标】 1、知道“物质的量”是描述微观粒子集体的物理量,摩尔是物质的量的基本单位 2、知道摩尔质量的概念和不同粒子的摩尔质量的计算方法 【能力目标】 1、学会有关物质的量的简单计算,理解物质的质量、摩尔质量、物质的量、物质的粒子数之间的相互关系及有关计算 2、通过学习,了解概念的形成过程及形成条件 【道德情感目标】在化学概念的学习过程中,体验类比、迁移的学习方法,培养思维能力以及研究问题的能力 二、重点与难点 【重点】物质的量的概念及其与摩尔质量、质量等之间的关系 【难点】物质的量、摩尔质量、质量等之间的关系 三、教学器材 投影仪 四、教学方法与过程 讨论法、归纳法 〖引入〗思考并讨论: 1、 问题1:一个个的水分子看得见吗?数得出吗?问题2:怎么比较谁喝的水多? 2、我们在初中学过了化学方程式,你能说出一个具体的化学方程式所代表的意义吗? ,方程式中的系数2是什么意义?我们如何取用二个碳原子与一个氧气分子反应? 〖讲解〗显然,我们能够很快想到可以用一定数目的粒子集体将宏观与微观联系起来,为此,
国际科学界引进了“物质的量”这样一个物理量(n),其单位为摩尔(mol),简称为摩。〖阅读〗P12资料卡片 〖过渡〗那么到底用多少粒子作为一个集体最为合适呢? 〖活动〗参照P11表格中的数据,学生进行猜想。 〖设问〗科学家选择了6.02×1023这样的近似数据,用此数据的优点是什么呢? 大量实验证明,约6.02×1023个粒子的质量都是以克为单位,数值上等于该粒子的相对原子质量或相对分子质量。所以我们就把含有约6.02×1023个粒子集体计量为1mol,也就是说1 mol任何粒子所含粒子数约为6.02×1023个,这里的粒子集体可以是原子、分子、离子或原子团,也可以是电子、质子、中子等,但不可以是宏观物体。 〖举例〗1 molFe、1 molO2、1 molNa+、1molSO42—、2molH2O 指出注意事项:使用摩尔作为单位时,所指粒子必须十分明确,且粒子的种类要用化学式表示。 〖讲解〗阿伏加德罗是意大利物理学家,他对6.02×1023这个数据的得出,有着很大的贡献,故用其名字来表示该常数,以示纪念,即将6.02×1023 mol-1叫做阿伏加德罗常数,用N A表示。 〖归纳〗归纳得出公式:粒子数N=n?N A 〖练习〗 5molH2SO4中含有的分子个数是多少?原子总数是多少?氧原子个数是多少? 1、0.5 molNa2SO4中含有________mol Na+;_________SO42-;___________mol O。 2、下列叙述正确的是: A:同质量的H2和Cl2相比,H2的分子数较多。 B:1 mol 大米含有6.02 ×1023米粒。 C:摩尔是物质的数量单位。 D:1 mol Na变成Na+失去的电子数为 6.02 ×1023个。 3、有如下物质,按要示填空: ①0.7 mol HCl ②0.2 mol NH3③3.01×1023 H2O ④6.02×1022CH4 比较上述物质所含分子数的多少,按多到少的顺序排列。 比较上述物质所含原子数的多少,按多到少的顺序排列。 比较上述物质所含H原子数的多少,按多到少的顺序排列。
常见物质的摩尔质量表
摩尔质量 化合物 M 化合物 M (g ? moI -1) 化合物 M / (g ? moI -1 ) / (g - moI-1) AgAsQ FeSO? 7H2O (NHL) 2QQ AgBr Fe(NH)2(SO)2 ? 6H2O (NH)2G Q ?H2O AgCl H B A S O NHSCN AgCN HAO NHHCO AgSCN HBO (NHO2M0O AICI3 HBr NHNO Ag2CrO4 HCN (NHO2HPO AgI HCOOH (NH L)2S AgNO CHCOOH (NHO2SO AICI3 ? 6HO H2CO NHVO AI(NO3)3 H2GQ NaAsQ AI(NO3)3 ? 9H2O H2C2C4 ? 2H2O N Q BO AI2O HCHQ (丁二酸) N Q BQ? 10H2O AI(OH)3 "GHQ (酒石酸) NaBiQ Al2(SQ)3 fGHsQ ? H O (柠檬酸) NaCN Al2(SO)3 ? 18H2O "GHQ (DL-苹果酸) NaSCN As?O HGHNO Na;CO
(DL-a-丙氨酸) As2Q HCl NaCO? 1OHO AS2S3 BaCO HF HI NaCQ CHCOONa BaGQ BaCl2 HIQ HNO CHCOONa3H2O NaCHQ (柠檬酸钠) BaCl2 ? 2H2O HNO NaCHNO ?H2O (L-谷氨酸钠) BaCrO H2O NaCl BaO H2Q NaClO Ba(OH) BaSO HPQ H2S NaHCO NaHPO? 12HO BiCl a H2SO NQHC o HkQN b (EDTA二钠盐) BiOCl H2SO Nc fe H2C io Hi2^N>. 2H2O CO Hg(CN:2 NaNO CaO HgCb NaNO CaCO HgC" NaO CaCC4 Hgl2 NaO2 CaCb Hg(NQ) 2 NaOH CaCb ? 6H2O Hg(NQ)2 ? 2HO NaPQ Ca(NO)2 ? 4HO Hg(NO)2 N Q S
木材横纹与顺纹实验报告剖析
木材横纹与顺纹压缩实验 摘要:为了解影响木材压缩性能的一些因素和机制并测量横纹与顺纹的弹性模量,抗拉强度以及比较二者的区别。本文用两块取自横纹和顺纹两个不同方向的木块的压缩试验结果做了一个对比,简要分析了不同构造的木材其不同的压缩力学性能,得到了两个不同方向的应力-应变特性曲线,证实了木材的各向异性以及得到了木材横纹和顺纹的力学性能。 关键词:木材各向异性;横纹方向; 顺纹方向 1.引言:我国森林覆盖率较低,木材资源较为匮乏,研究木材的压缩特性有助于让不同性能的木材各尽其用,节约成本。生活中,人们对木材这种材料有着非常感性的认识,比如“劈柴沿着顺纹方向比较轻松”、“砍树要比劈柴费劲得多”。事实上,木材是一种极为特殊的各向异性多孔材料,作为一种天然的复合材料,在外加载荷作用下有着非常复杂的力学特性。木材微观上由许多含有空腔的细胞所组成。其中近于沿树干主轴方向排列者占绝大多数,该方向称为轴向或顺纹方向;而与树干主轴相垂直的方向,包括径向、弦向、半弦向等,统称为横纹方向。 2.试验方案: 2.1使用设备 WDW-3050电子万能试验机、光学引伸计、计算机、游标卡尺、横纹木材试件、顺纹木材试件各一件。 2.2试样
2.3实验原理 2.3.1 木材的微观组成 木材由纤维素、半纤维素和木质素三大组分构成。组成木材细胞壁的主要化学成分,按其物理作用可分为3类:骨架物质、基体物质和结壳物质。有人形象的将骨架物质、基体物质、结壳物质分别比作钢筋、沙石、水泥。 骨架物质:以纤维素的微纤丝状态存在于细胞壁中,赋予细胞拉压强度。纤维素为线形、长的大分子结构,其分子链不是笔直成线,而是具有一定程度的卷曲,这就决定了纤维素具有可以伸缩的弹性性能。纤维素作为木材的骨架结构元素,其含量主要影响木材的刚度。 基体物质:指半纤维素和其它碳水化合物。渗透于骨架物质,增加细胞的刚性。结壳物质:指木质素,遍布于细胞壁之中,使细胞获得硬度。 1.测量试样原始尺寸:用游标卡尺测量试件基本尺寸,如标记段原始长度,宽度,厚度, 多测几次取平均。由于要使用光学引伸计,应该用快干墨水或带色涂料标出两个标记点。 2.试验机准备:预先开动试验机,确定试验机工作正常。打开相机,确认图像可以正常采 集。
摩尔质量
化学计量在实验中的应用(第1课时) 1.下列说法正确的是() A.物质的量表示物质数量的多少 B.物质的量就是物质的质量 C.摩尔是表示微观粒子的数目 D.摩尔是物质的量的单位 2.下列说法错误的是() A.1 mol 氢 B.1 mol O C.1 mol 二氧化碳 D.1 mol水 3.0.5 molNa2SO4中含有Na+的数目是()个 A.3.01×1023 B.6.02×1023 C.0.5 D.1 4.下列说法正确的是() A.1 molH2的质量是1 g B.1 mol HCl的质量是36.5 g·mol-1 C.Cl2的摩尔质量等于它的相对分子质量 D.硫酸根离子的摩尔质量是96 g·mol-1 5.下列叙述正确的是() A.1 mol氧含有约6.02×1023个氧原子 B.1 mol12C的质量是12 g C.0.1 mol H2SO4含有氢原子数精确值为1.204×1022 6.设N A为阿伏加德罗常数的值,下列说法不正确的是() A. 1 mol甲烷和N A个甲烷分子的质量相等 B.0.1 mol Na+、NH3、OH-、F-均含有N A个电子 C.N A个O2分子和N A个O3分子质量相等 D.N A个O2和N A个H2的质量比是16∶1 7.在空气中的自由离子附着在分子或原子上形成的空气负离子被称为“空气维生素”。O2-2就是一种空气负离子,则O2-2的摩尔质量为() A.32g B.34g C.32g/mol D.34g·mol—1 8.下列说法正确的是() A.摩尔是一种国际基本物理量 B.氢气的摩尔质量为2g C.氧气的气体摩尔体积约为22.4L D.阿伏加德罗常数的符号为N A,近似值为6.02×1023 mol-1 9.下列叙述中正确的是() A.摩尔是物质的量的单位,毎摩尔物质含有6.02×1023个分子 B.1 mol氧的质量为16 g C.0.5 mol氦气约含有6.02×1023个电子 D.2H既可表示2个氢原子又可表示2 mol氢分子 10.下列物质的摩尔质量最大的是() A.10 mL H2O B.0.8 mol H2SO4 C.54 g Al D.1 g CaCO3 11.O2、SO2、SO3三者的质量比为2∶4∶5时,它们的物质的量之比为()
迈克尔逊干涉仪实验报告
迈克尔逊干涉仪(实验报告) 一、实验目的 1、掌握迈克尔逊干涉仪的调节方法并观察各种干涉图样。 2、区别等倾干涉、等厚干涉和非定域干涉,测定He-Ne 激光波长 二、实验仪器 迈克尔逊干涉仪、He-Ne 激光器及光源、小孔光阑、扩束镜(短焦距会聚镜)、毛玻璃屏等。 (图一) (图二) 三、实验原理 ①用He-Ne 激光器做光源,使激光通过扩束镜会聚后发散,此时就得到了一个相关性很好的点光源,射到分光板P1和P2上后就将光分成了两束分别射到M1 和M2 上,反射后通过P1 、P2 就可以得到两束相关光,此时就会产生干涉条纹。 ②产生干涉条纹的条件,如图2 所示,B 、C 是两个相干点光源,则到A 点的光程差δ =AB-AC=BCcosi , 若在A 点出产生了亮条纹,则δ =2dcosi=k λ (k 为亮条纹的级数) ,因为i 和k 均为不可测的量,所以取其差值,即λ =2 Δ d/ Δ k? 。 四、实验步骤 1、打开激光电源,先不要放扩束镜,让激光照到分光镜P1 上,并调节激光的反射光照射到激光筒上。 2、调节M2 的位置使屏上两排光中最亮的两个光点重回,并调至其闪烁。 3、将扩束镜放于激光前,调节扩束镜的高度和偏角,使光能照在P1分光镜上,看显示屏上有没有产生同心圆的干涉条纹图案。没有的话重复2 、3 步骤,直到产生同心圆的干涉条纹图案。 4、微调M2是干涉图案处于显示屏的中间。 5、转动微量读数鼓轮,使M1 移动,可以看到中心条纹冒出或缩进,若看不到此现象,先转动可度轮,再转动微量读数鼓轮。记下当前位置的读数d0 ,转动微量读数鼓轮,看到中心条纹冒出或缩进30 次则记一次数据,共记录10 次数据即d0、d1 (9) 6、关闭激光电源,整理仪器,处理数据。 五、实验数据处理 数据记录: 数据处理: Δd0=d5-d0=0.05202mm??????? Δd1=d6-d1=0.05225mm Δd2=d7-d2=0.04077mm??????? Δd3=d8-d3=0.04077mm Δd4=d9-d4=0.05071mm Δd(平均)=(Δd0+Δd1+Δd2+Δd3+Δd4)/5 =0.047304mm
高一化学摩尔教案
高一化学《摩尔》教案: 知识目标 使学生在理解,特别是标准状况下,的基础上,掌握有关的计算。 能力目标 通过的概念和有关计算的教学,培养学生分析、推理、归纳、总结的能力。 通过有关计算的教学,培养学生的计算能力,并了解学科间相关知识的联系。 情感目标 通过本节的教学,激发学生的学习兴趣,培养学生的主动参与意识。 通过教学过程中的设问,引导学生科学的思维方法。 [板书] 二、有关的计算 [讨论] 气体的体积与气体的物质的量、气体的质量和气体中的粒子数目之间的关系:(由学生回答) [板书] 1. 依据:和阿伏加德罗定律及其推论 2.类型 (1)标准状况下气体的体积与气体的物质的量、气体的质量和气体中的粒子数目之间的关系 [投影] 例题1:在标准状况下,2.2gCO2的体积是多少? [讨论] 1.由学生分析已知条件,确定解题思路。 2.学生在黑板上或练习本上演算。 [强调] 1.解题格式要求规范化。 2.计算过程要求带单位。 [板书](2)气体相对分子质量的计算 [投影] 例题2:在标准状况下,测得1.92g某气体的体积为672mL。计算此气体的相对分子质量。 [讨论] 分析已知条件首先计算气体的密度:= 然后求出标准状况下22.4L气体的质量,即1mol 气体的质量:M= Vm [学生解题] 分析讨论不同的解法。 [投影] 例题3:填表 [练习]若不是标准状况下,可以利用阿伏加德罗定律及其推论解题。 某气体对氢气的相对密度为14,求该气体的相对分子质量。 [分析]由于是同温同压,所以式量的比等于密度比。 [板书](3)混合气体 [投影] 例题3:已知空气中氮气和氧气的体积比为4 :1,求空气的平均相对分子质量。 [分析] 已知混合气体的组成,求其相对分子质量,应先求出混合气体的平均摩尔质量。如用n1、n2表示混合物中各组分的物质的量;M1、M2表示混合物中各组分的摩尔质量;V1、V2表示混合物中各组分的体积,则混合气体的平均摩尔质量可由下面的公式求得:
光学实验报告 (一步彩虹全息)
光学设计性实验报告(一步彩虹全息) 姓名: 学号: 学院:物理学院
一步彩虹全息 摘要彩虹全息是用激光记录全息图, 是用白光再现单色或彩色像的一种全息技术。彩虹全息术的关键之处是在成像光路( 即记录光路) 中加入一狭缝, 这样在干板上也会留下狭缝的像。本文研究了一步彩虹全息图的记录和再现景象的基本原理、一步彩虹全息图与普通全息图的区别和联系、一步彩虹全息的实验光路图,探讨了拍摄一步彩虹全息图的技术要求和注意事项,指出了一步彩虹全息图的制作要点, 得出了影响拍摄效果的佳狭缝宽度、最佳狭缝位置及曝光时间对彩虹全息图再现像的影响。 关键词:一步彩虹全息;狭缝;再现 1 光学实验必须要严密,尽可能地减少实验所产生的误差; 2 实验仪器 防震全息台激光器分束镜成像透镜狭缝干板架光学元件架若干干板备件盒洗像设备一套线绳辅助棒扩束镜2个反射镜2个 3 实验原理 3.1 像面全息图 像面全息图的拍摄是用成像系统使物体成像在全息底板上,在引入一束与之相干的参考光束,即成像面全息图,它可用白光再现。再现象点的位置随波长而变化,其变化量取决于物体到全息平面的距离。 像面全息图的像(或物)位于全息图平面上,再现像也位于全息图上,只是看起来颜色有变化。因此在白光照射下,会因观察角度不同呈现的颜色亦不同。 3.2 彩虹全息的本质 彩虹全息的本质是要在观察者与物体的再现象之间形成一狭缝像,使观察者通过狭缝像来看物体的像,以实现白光再现单色像。若观察者的眼睛在狭缝像附近沿垂直于狭缝的方向移动,将看到颜色按波长顺序变化的再现像。若观察者的眼睛位于狭缝像后方适当位置, 由于狭缝对视场的限制, 通过某一波长所对应的狭缝只能看到再现像的某一条带, 其色彩与该波长对应, 并且狭缝像在空间是连
- 无机化学实验第四版实验二十一:ds区金属(铜,银,锌,镉,汞)
- 无机化学实验第四版实验2铁钴镍
- 无机化学实验第四版实验六:二氧化碳相对分子质量的测定实验报告
- 北师大《无机化学》第四版习题答案——下册
- 最新无机化学实验第四版实验24 铁钴镍资料
- 无机化学实验第四版实验24铁钴镍
- 无机化学实验第四版实验二十一:ds区金属(铜,银,锌,镉,汞)知识讲解
- 无机化学实验第四版实验24 铁钴镍
- 无机化学实验第四版实验十八:p区非金属元素(二)(卤素,氧,硫)
- 无机化学 第四版 (杨宏孝 王建辉 著) 高等教育出版社 课后答案
- 无机化学实验第四版实验二十一:ds区金属(铜-银-锌-镉-汞)
- 无机化学实验第四版实验十八:p区非金属元素(二)(卤素-
- 无机化学实验第四版实验十八:p区非金属元素(二)(卤素,氧,硫)
- 无机化学实验第四版实验24 铁钴镍
- 无机化学实验第四版实验24铁钴镍
- 无机化学实验第四版实验二十一ds区金属铜
- 无机化学第四版(北京师范大学大学等)答案——下册
- 无机化学实验第四版实验二十一:ds区金属(铜,银,锌,镉,汞)
- 无机化学实验第四版实验十八:p区非金属元素(二)(卤素,氧,硫)
- 无机化学实验第四版实验二十一:ds区金属(铜,银,锌,镉,汞)
