【CN110358807A】果糖基赖氨酸的测定方法【专利】

(19)中华人民共和国国家知识产权局
(12)发明专利申请
(10)申请公布号 (43)申请公布日 (21)申请号 201910279861.0
(22)申请日 2019.04.09
(30)优先权数据
2018-075805 2018.04.11 JP
2018-173216 2018.09.18 JP
(71)申请人 池田食研株式会社
地址 日本广岛县
(72)发明人 佐藤大祐 竹中涼
(74)专利代理机构 北京集佳知识产权代理有限
公司 11227
代理人 苗堃 金世煜
(51)Int.Cl.
C12Q 1/48(2006.01)
C12N 9/12(2006.01)
C12N 9/96(2006.01)
(54)发明名称
果糖基赖氨酸的测定方法
(57)摘要
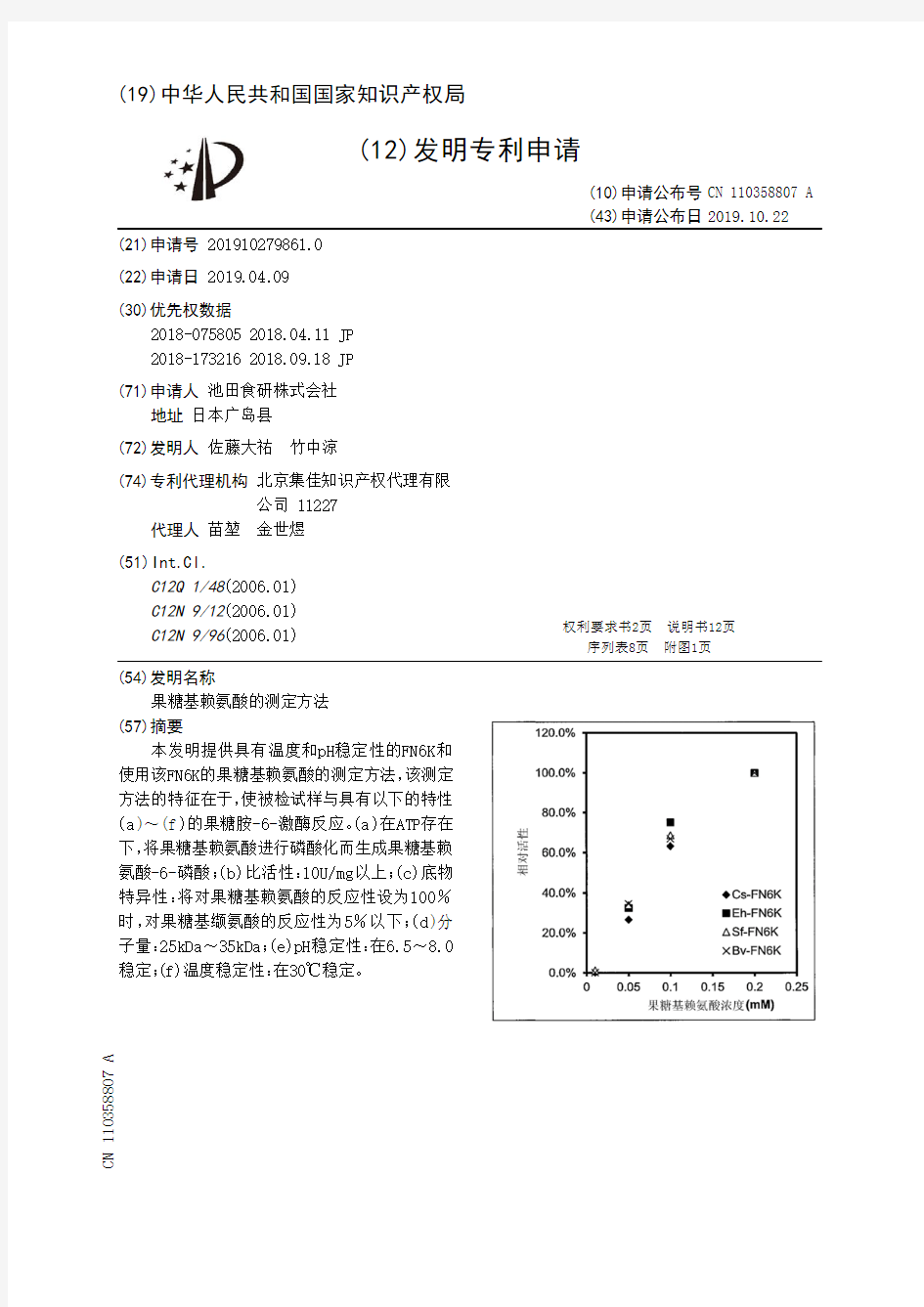
本发明提供具有温度和pH稳定性的FN6K和
使用该FN6K的果糖基赖氨酸的测定方法,该测定
方法的特征在于,使被检试样与具有以下的特性
(a )~(f )的果糖胺-6-激酶反应。(a )在ATP存在
下,将果糖基赖氨酸进行磷酸化而生成果糖基赖
氨酸-6-磷酸;(b)比活性:10U/mg以上;(c)底物
特异性:将对果糖基赖氨酸的反应性设为100%
时,对果糖基缬氨酸的反应性为5%以下;(d )分
子量:25kDa~35kDa;(e)pH稳定性:在6.5~8.0
稳定;(f)温度稳定性:
在30℃稳定。权利要求书2页 说明书12页序列表8页 附图1页CN 110358807 A 2019.10.22
C N 110358807
A
权 利 要 求 书1/2页CN 110358807 A
1.一种果糖基赖氨酸的测定方法,其特征在于,使被检试样与具有以下的特性(a)~
(f)的果糖胺-6-激酶反应,
(a)在ATP存在下,将果糖基赖氨酸进行磷酸化而生成果糖基赖氨酸-6-磷酸;
(b)比活性:10U/mg以上;
(c)底物特异性:将对果糖基赖氨酸的反应性设为100%时,对果糖基缬氨酸的反应性为5%以下;
(d)分子量:25kDa~35kDa;
(e)pH稳定性:在6.5~8.0稳定;
(f)温度稳定性:在30℃稳定。
2.根据权利要求1所述的果糖基赖氨酸的测定方法,其中,果糖胺-6-激酶进一步具有以下的特性(g)和(h),
(g)最适活性pH:8.0~8.5,
(h)最适活性温度:35~40℃。
3.根据权利要求1或2所述的果糖基赖氨酸的测定方法,其特征在于,测定温度为35℃以上。
4.根据权利要求1~3中任一项所述的果糖基赖氨酸的测定方法,其特征在于,在pH
5.0~9.0的范围内测定。
5.一种果糖基赖氨酸测定用试剂,含有具有以下的特性(a)~(f)的果糖胺-6-激酶,
(a)在ATP存在下,将果糖基赖氨酸进行磷酸化而生成果糖基赖氨酸-6-磷酸;
(b)比活性:10U/mg以上;
(c)底物特异性:将对果糖基赖氨酸的反应性设为100%时,对果糖基缬氨酸的反应性为5%以下;
(d)分子量:25kDa~35kDa;
(e)pH稳定性:在6.5~8.0稳定;
(f)温度稳定性:在30℃稳定。
6.根据权利要求5所述的果糖基赖氨酸测定用试剂,其中,果糖胺-6-激酶进一步具有以下的特性(g)和(h),
(g)最适活性pH:8.0~8.5,
(h)最适活性温度:35~40℃。
7.一种果糖基赖氨酸测定用试剂盒,包含具有以下的特性(a)~(f)的果糖胺-6-激酶,
(a)在ATP存在下,将果糖基赖氨酸进行磷酸化而生成果糖基赖氨酸-6-磷酸;
(b)比活性:10U/mg以上;
(c)底物特异性:将对果糖基赖氨酸的反应性设为100%时,对果糖基缬氨酸的反应性为5%以下;
(d)分子量:25kDa~35kDa;
(e)pH稳定性:在6.5~8.0稳定;
(f)温度稳定性:在30℃稳定。
8.根据权利要求7所述的果糖基赖氨酸测定用试剂盒,其中,果糖胺-6-激酶进一步具有以下的特性(g)和(h),
2
pH值对赖氨酸保护作用影响的研究
pH值对赖氨酸保护作用影响的研究1 贺洪1、2,刘慧敏2,朱泽瑞2,印大中2 1 湖南师范大学体育学院,湖南长沙(410012) 2 湖南师范大学生命科学学院,湖南长沙(410081) 摘要:用紫外吸收研究力竭运动后大鼠血清中赖氨酸(lysine)对丙二醛(MDA)的清除。通过试管反应发现,在适宜的浓度和pH值下,赖氨酸能与MDA结合形成类似尿液的成分;乳酸升高所营造的微酸性环境能促使这一反应的进行。提示:剧烈运动前后适时适量饮用赖氨酸能抵抗氧应激代谢产物的生物毒性作用,保护机体免受伤害。 关键词:赖氨酸,丙二醛,运动保护 脂质过氧化中间产物MDA、HNE(4-羟基壬烯醛)等不饱和醛酮具有生物活性,能与含氮生物分子发生交联,使动物组织硬化,造成伤害[1-6]。所以MDA的代谢途径早就成为科学家们研究的热点。在小鼠和人类的尿液中寻找MDA的分泌物,发现MDA在尿液中主要是以与赖氨酸结合的两种物质的形式—N-ε-2-丙烯醛赖氨酸和N-α-乙酰酯存在[7]。这就表明在体内MDA主要是作用于蛋白质中的赖氨酸残基。本文采用体外试管实验考察赖氨酸和MDA的反应产物以及pH值对反应速率的影响。 1. 材料和方法 1.1 试剂 ≧;盐酸赖超纯水,由Milli-Q系统纯化(Millipore China Limited), 电导率18.2M?.cm 氨酸购于长沙瑞晶生物经营部;TMP购于sigma公司;其他均为常规试剂。 1.2 试剂的配制 1.2.1 磷酸缓冲液(PBS)取0.2 mol/L Na2HPO4.12H2O和0.2 mol/L NaH2PO4.2H2O1配制pH7.4、7.2、7.0、6.8的PBS缓冲液。 1.2.2 16 mmol/L赖氨酸称取四份赖氨酸0.2952 g,于少量超纯水中溶解,用6 mol/L NaOH 调节pH值至7.4、7.2、7.0、6.8。以相应pH值的PBS溶液定容至100 ml。 1.2.3 1 mmol/L MDA[8]用四个50 mL容量瓶分别加1 mol /L HCl 2 mL,再加0.00845 mL TMP,于40℃水浴溶解,精确计时2.5 min后取出,分别用6 mol/L的NaOH调pH至7.4、7.2、7.0、6.8。最后用相应pH值的PBS溶液定容至50 mL。 1.3 仪器设备 PT电动跑台(浙江省杭州立泰科技有限公司);Lambda Bio45紫外分光光度仪(美国Perkin Elmer公司);D-37520型高速冷冻离心机(德国Heraeus Biofuge公司);Molli-Q Academic A 10超纯水系统(Millipore China Limited);Mettler Toledo A E200分析天平(上海梅特勒—托利多有限公司)。 1.4 MDA和赖氨酸的试管反应 1.4.1测定赖氨酸、MDA、力竭大鼠尿液和赖氨酸与MDA反应产物的紫外吸收光谱图将1 mmol/L的赖氨酸、0.01 mmol/L的MDA、即刻取得的力竭大鼠的尿液、16 mmol/L的赖氨1本课题得到湖南师范大学体育学院课题经费资助(课题号:JS0603)
羟基自由基的测定方法
羟基自由基(.OH)是最活跃的一种活性分子,也是进攻性最强的化学物质之一,几乎可以与所有的生物分子、有机物或无机物发生各种不同类型的化学反应,并伴有非常高的反应速率常数和负电荷的亲电性。羟基自由基是目前所知活性氧自由基中对生物体毒性最强、危害最大的一种自由基,可以通过电子转移、加成以及脱氢等方式与生物体内的多种分子作用,造成糖类、氨基酸、蛋白质、核酸和脂类等物质的氧化损伤,使细胞坏死或突变,羟基自由基还与衰老、肿瘤、辐射损伤和细胞吞噬等有关。羟基自由基由于其寿命短,反应活性高,存在浓度低,目前尚未有专一、有效的方法可以精确测定羟基自由基的含量,其测定方法也成为一项国际性的难题。本文对近几年出现的羟基自由基检测方法进行了综述。 1电子自旋共振法 电子自旋共振法或电子顺磁共振法主要研究对象为未成对的自由基或过渡金属离子及其化合物。自旋捕捉(spin trapping)技术的出现为化学反应中自由基中间体及生命活动过程中短寿命自由基的检测开辟了新的检测途径[[1]]。此方法是利用捕捉剂与自由基结合形成相对稳定的自旋加合物(spin adducts),然后进行ESR测定。 2HPLC法 HPLC法可用于间接测定自由基。测定过程中必须先选择合适的化合物捕集被测体系中的自由基,使之生成具有一定稳定性,且能被液相色谱分离与检测的产物,然后用HPLC进行测定。1)、采用二甲基亚砜捕集羟基自由基的HPLC测 2)、采用水杨酸捕集羟基自由基的HPLC测定方法 3化学发光法 化学发光法是一种灵敏、准确的检测自由基的方法,其原理是利用发光剂被活性氧自由基氧化成激发态,当其返回到基态时放出大量光子,从而对发光起放大作用。且自由基产生越多,发光值就越大。通过函数换算间接反应系统中自由基的量。与ESR和HPLC法相比,具有操作简便、设备成本较低、测定快速等优点。4氧化褪色光度法 6极谱法 7毛细管电泳-电化学检测法 8胶束电动毛细管色谱法
自由基及检测方法
ESR 电子顺磁共振(EPR)或称电子自旋共振(ESR)现象最早发现于1944年。它利用具有未成对电子的物质在磁场作用下吸收电磁波的能量使电子发生能级间的跃迁的特征,对顺磁性物质进行检测与分析。 自旋捕集方法是将不饱和的抗磁性化合物(自旋捕集剂)加入反应体系,与反应体系中产生的各种活性高、寿命短的自由基结合形成相对稳定的自旋加合物,以适于ESR检测其原理是利用适当的自旋捕捉剂与活泼的短寿命自由基结合,生成相对稳定的自旋加合物,可以用电子自旋共振波谱法检测自旋加合物的数量,利用自旋加合物的数量来计算原来自由基的多少。 H: V: ESR测自由基是怎么被检测的(细胞,组织,溶液?体内,体外?) (MGD)2 - Fe2 +,是含有10mmol·L- 1MGD 和2mmol·L- 1FeSO4的溶液。 体外捕集:处死后取组织(血液、细胞),加入捕集剂,ESR测定 体内捕集:腹腔注射捕集剂,处死取组织(血液、细胞),ESR测定 腹腔注射几乎没有检测到自由基信号,或者信号很弱,而处死后样品加捕获剂则可以检测到自由基信号。 通用捕获剂 典型的自旋捕捉剂是亚硝基化合物或氮氧化合物,把足够量的自旋捕捉剂加入到产生自由基的体系中,自旋捕获剂就会快速地和任何出现的自由基反应,最后给出稳定的可检测的氮样氧自由基加合物。所形成的自由基加合物的ESR 谱上有被捕自由基基因给出的超精细分裂,可鉴别被捕自由基通用自旋捕获剂所形成的自由基加合物对自由基结构变化相当敏感, ESR 技术检测O-2 O-2可以与1,2-二羟基苯-3,5-二磺酸钠(Tiron)(钛铁试剂)快速反应生成一种称之为“Tiron 半醌自由基”的自旋加合物,比较稳定,可在室温下应用电子顺磁共振波谱仪(EPR)进行检测,从而解决了生理条件下水溶液中寿命极其短暂的O-2·的定性和定量问题 ESR 技术检测·OH DMPO作自由基捕获剂对自由基结构变化相当敏感,可以提供自由基结构的详细信息。它与·OH产生的自旋加合物的ESR谱表现出特别容易识别的特征谱线。在溶液中容易形成的自我捕集产物二聚体自由基不会干扰实验结果。 ESR 技术检测血红蛋白结合的一氧化氮 在组织或血液中,一氧化氮大多与氧或过渡金属反应生成了硝酸盐或亚硝酸盐以及一氧化氮与金属的配合物。一氧化氮与血红蛋白的结合速率常数非常高,而且能够得到有特征的ESR 波谱。利用这一性质,我们可以用血红蛋白作为一氧化氮的捕集剂检测一氧化氮自由基。但是,HbNO 极易氧化,这就限制了这种方法在富氧条件下的应用。 ESR 技术检测生物体系产生的一氧化氮 一氧化氮与含金属蛋白反应产生的亚硝酰的金属配合物,往往会抑制细胞中许多重要的酶,对细胞产生毒害作用。目前应用较多的捕集剂的有Fe2+- (DETC)2,它可与一氧化氮形成稳定的单亚硝酰-铁配合物MNIC,给出特征的ESR 波谱。但由于Fe2+-( DETC)2不溶
赖氨酸发酵生产
赖氨酸发酵生产 摘要:赖氨酸是人体必需的八大氨基酸之一,能促进人体发育、增强免疫功能,并有提高中枢神经组织功能的作用。赖氨酸为碱性必需氨基酸。由于谷物食品中的赖氨酸含量甚低,且在加工过程中易被破坏而缺乏,故称为第一限制性氨基酸。将赖氨酸添加到食品中能大大提高蛋白质的利用率,又是一种优良的食品强化剂。因此研究赖氨酸的生产有着很高的价值。关键词: 简介: 赖氨酸是一种碱性氨基酸,是仅次于谷氨酸的第二大氨基酸产品,是谷物蛋白的第一限制性氨基酸,在谷物食料中添加适量的赖氨酸,其蛋白质的生物价大大提高。 赖氨酸的应用范围很广。①作为食品强化剂;②作为药物可用作肝细胞再生剂,对改善肝功能,治疗肝硬化、高氨症,增进食欲、改善营养状况有明显的疗效;③作为饲料添加剂,在畜、禽类的饲料中添加少许的赖氨酸,对家禽、家畜的日增重、料肉比、家禽的产卵量等方面效果尤为显著。 1.赖氨酸发酵机制 赖氨酸合成途径的调节机制 (1)谷氨酸优先合成,谷氨酸合成过剩就会抑制谷氨酸脱氢酶(GD)的活性,使得生物合成的代谢流转向天门冬氨酸。天门冬氨酸的过剩也会抑制磷酸烯醇式丙酮酸羧化酶的活性,使得天门冬氨酸不致大量积累。 (2)赖氨酸的前体物质天门冬氨酸与乙酰辅酶A的生成形成平衡合成,乙酰辅酶A的增加能逆转天门冬氨酸对其自身合成的反馈抑制。 (3)天门冬氨酸激酶(AK)受赖氨酸与苏氨酸的协同反馈。AK是一个变构酶,催化天门冬氨酸和ATP形成α-天门冬氨酸磷酸,有两个变构位置可以接受末端产物。AK受赖氨酸与苏氨酸的协同抑制,当只有赖氨酸或苏氨酸与变构位置结合时,酶活影响不大,当赖氨酸与苏氨酸同时结合到两个变构位置时,酶活受到强烈的抑制。此外,AK是赖氨酸合成途径中唯一的反馈调节点。 (4)赖氨酸亮氨酸的生物合成之间存在着代谢互锁,赖氨酸分支途径的初始酶二氢吡啶二
谷物种子蛋白质中赖氨酸含量的测定
谷物种子蛋白质中赖氨酸含量的测定 一、实验目的 掌握茚三酮比色法测定氨基酸含量的原理和方法,测定谷物种子蛋白质中赖氨酸含量。 二、实验原理 蛋白质中的赖氨酸具有一个游离的ε-NH2,它与茚三酮试剂反应生成蓝紫色物质,其颜色的深浅在一定范围内与赖氨酸的含量成线性关系。因此,用已知浓度的游离氨基酸制作标准曲线,通过比色分析(530nm)即可测定出样品中的赖氨酸含量。 亮氨酸与赖氨酸的碳原子数目相同,而且仅有—个游离氨基(ε-NH2),所以通常用亮氨酸配制标准液。但由于这两种氨基酸分子质量不同,以亮氨酸为标准计算赖氨酸含量时,应乘以校正系数1.1515,最后再减去样品中游离氨基酸含量。 三、实验仪器 1.电子分析天平(1/1000)、可见分光光度计、恒温水浴箱、干燥器、移液器。 2.试管架(塑及铝)、具塞试管、具塞三角瓶、细口瓶、漏斗(或0.45um滤膜)、吸管等。 四、实验试剂 1.0.4mol/L柠檬酸缓冲液:称取4.202g柠檬酸和5.88g柠檬酸三钠,溶于100ml蒸馏水中。 2.茚三酮试剂:称40mg二氯化锡(防腐)溶于25ml柠檬酸缓冲液中;称lg 茚三酮溶于25ml 95%乙醇中;将上述两液混合摇匀,滤去沉淀,上清液置冰箱中保存备用。 3.0.02mol/L盐酸:取12mol/L盐酸0.17ml,用蒸馏水稀释定容至100ml。4.亮氨酸标准液:准确称取20mg亮氨酸,加数滴0.02mol/L盐酸使之溶解,然后用蒸馏水稀释定容到100ml,则得浓度为200μg/ml的标准液。5.60%乙醇。 6.4%碳酸钠:称取4g无水碳酸钠,溶于100 ml蒸馏水。 7.2%碳酸钠。
L-赖氨酸的生产工艺研究
L-赖氨酸的发酵生产工艺研究 摘要: L-赖氨酸是人体和动物所不能合成的八种必需氨基酸中最重要的一种。L-赖氨酸是国际市场上发展前景良好的产品,消费需求每年以7-10%的速度递增,国内年产量则以每年20-30%以上的速度递增。其广泛应用于医药、食品和饲料等领域。目前生产赖氨酸最主要的方法是微生物发酵法。本文从赖氨酸的生产现状、生产方法,发酵过程中的代谢调控以及赖氨酸生产菌种的选育和生产赖氨酸的前景展望这几个方面综述了赖氨酸生产工艺。 关键词: 赖氨酸;发酵;菌种;展望 前言 赖氨酸(Lysine) 的化学名称为2,6-二氨基己酸,有L-型(左旋)、D-型(右旋)和DL 型(消旋)三种旋学异构体。赖氨酸是人和动物营养的必需氨基酸之一,不能参加转氨作用[1]。人类和动物可吸收利用的只有L型。它对调节体内代谢平衡、提高体内对谷类蛋白质的吸收、改善人类膳食营养和动物营养、促进生长发育均有重要作用。L-赖氨酸主要用于医药、食品和饲料工业。全球约9 0%的赖氨酸用作饲料添加剂,约5%用作食品添加剂,其余5%用作医药中间体[2]。目前,全球赖氨酸年总需求量约为85万t/a,年增长率为7%一8%。现全球赖氨酸总产能约为80万t/a,产量较大的是日本味之素公司(26万t/a)、美国ADM公司、BASF韩国公司和协和发酵工业公司等。国内赖氨酸需求量估计在13万t/a左右。赖氨酸应用范围较广,2003年以后,我国已成为全球最大的赖氨酸生产大国。目前已建成和正在建设的赖氨酸厂主要有广西赖氨酸公司、福建大泉赖氨酸有限公司、四川川化味之素有限公司、大成赖氨酸厂、肇东赖氨酸厂等。文章从赖氨酸的生产现状、生产方法,发酵过程中的代谢调控以及赖氨酸生产菌种的选育和生产赖氨酸的前景展望等方面论述了赖氨酸生产工艺的研究进展。 1赖氨酸生产现状 L-赖氨酸最初是从蛋白质水解物中分离得到的,蛋白质水解法一般以动物血粉为原料,此法最多的特点是工艺流程简单,但是原料来源很有限,仅适合小规模生产。此后又出现了化学合成法、水解法,酶法。直到1960年,日本首先采用微生物发酵法生产赖氨酸。微生物发酵生产氨基酸是人为地解除氨基酸生物合成的代谢控制机制,使其积累大量所需氨基酸。氨基酸的L-型立体专一性决定了发
最新各类赖氨酸实际有效含量
各类赖氨酸产品分子式如下: 赖氨酸分子式:C6H14N2O2 赖氨酸硫酸盐分子式:[C6H14N2O2]2·H2SO4 赖氨酸盐酸盐分子式:C6H14N2O2·HCL 既然有了分子式,那么很容易算出,赖氨酸分子量是146.1886, 赖氨酸硫酸盐分子量是390.4490,赖氨酸盐酸盐分子量是182.6495。 分子量算出来了,那么很明显,针对赖氨酸硫酸盐([C6H14N2O2]2·H2SO4),其赖氨酸百分含量就是Lys%=(146.1886*2)/390.4490*100%=74.88%;针对赖氨酸盐酸盐(C6H14N2O2·HCL),其赖氨酸百分含量就是Lys%=146.1886/182.6495*100%=80.38%。 接下来再举发帖的楼主这个例子,拿70%的赖氨酸盐酸盐产品说事吧,------70%赖氨酸盐酸盐,就是指你所买的赖氨酸产品,是赖氨酸盐酸盐形式的,其中赖氨酸盐酸盐的纯度是70%(其余30%基本上是载体),那么折合下来其赖氨酸的实际含量就是Lys%=1*70%*80.38%=56.03%。 其它的算法都类似,不管它纯度是65%、70%、98.5%,也不管它是赖氨酸盐酸盐还是赖氨酸硫酸盐,折合出的赖氨酸实际当量,归根结底最后都是一个简单的数学换算,就不用一一列举了吧? 相关产品赖氨酸含量换算关系一览表 品名 赖氨酸盐酸盐赖氨酸硫酸盐 分子式C6H14N2O2·HCL [C6H14N2O2]2·H2SO4 纯品赖氨酸盐之赖氨酸含量80.04% 74.88% 65%纯度赖氨酸含量52.02% 48.67% 70%纯度赖氨酸含量56.03% 52.42% 98.5%纯度赖氨酸含量78.84% 73.76% 欣赏全国名师优秀课例心得体会 王健 这几天,我非常认真的观看了几位美术老师的优秀课例,通过学习名师的优秀课堂,让我受益匪浅。我被他们精彩的课堂设计、学生与老师之间的默契互动所吸引;被她们自然大方的教态所感染。让我从中学到了不少优秀的教学经验,为我今后在课堂教学中为创建高效课堂提供了很大的帮助。 这些课堂中都有一个共同点——“实在”,授课教师在讲课中,与学生打成一片,与学生的距离可谓是近之又近,没有花架子,他们
L赖氨酸的发酵方法与设计方案
本技术涉及发酵领域,具体提供了一种L赖氨酸的发酵方法,在赖氨酸一级种子培养基、赖氨酸二级种子培养基和赖氨酸发酵培养基中添加醋酸 盐,并优化了上述各培养基的配方和发酵工艺。本技术所提供的发酵方法,能够促进产赖氨酸菌体的生长和赖氨酸的合成,显著提高终点赖氨酸含 量、总酸量及糖酸转化率,并显著缩短发酵周期。 技术要求 1.一种L-赖氨酸的发酵方法,其特征在于,在赖氨酸一级种子培养基、赖氨酸二级种子培养基和赖氨酸发酵培养基中添加醋酸盐。 2.根据权利要求1所述的发酵方法,其特征在于,包括以下步骤: (1)赖氨酸一级种子培养:赖氨酸摇瓶种子接入赖氨酸一级种子培养基在一级种子罐中培养,一级种子罐中硫酸铵的初始浓度为8-12g/L,当一级种 子培养基中总糖浓度下降至8-15g/L时,停止培养,得成熟赖氨酸一级种子液; (2)赖氨酸二级种子培养:将成熟赖氨酸一级种子液接入赖氨酸二级种子培养基在二级种子罐中培养,二级种子罐中硫酸铵的初始浓度为10- 15g/L,当二级种子培养基中还原糖浓度下降至5-8g/L时,停止培养,得成熟赖氨酸二级种子液; (3)赖氨酸发酵培养:将成熟赖氨酸二级种子液接入赖氨酸发酵培养基中,在流加葡萄糖溶液和硫酸铵溶液的条件下,在发酵罐中发酵培养,发酵 罐中的硫酸铵初始浓度为9-14g/L,培养40-44小时,得到L-赖氨酸。 3.根据权利要求1或2所述的发酵方法,其特征在于,所述赖氨酸一级种子培养基包括:蔗糖20-40g/L,硫酸镁0.5-1.5g/L,磷酸二氢钾0.5-1.5g/L, 硫酸铵8-12g/L,酵母浸粉5-10g/L,苏氨酸0.4-0.6g/L,蛋氨酸0.4-0.6g/L,味精7-10g/L,丙酮酸钠0.5-0.8g/L,醋酸盐1-3g/L。 4.根据权利要求1或2所述的发酵方法,其特征在于,所述赖氨酸二级种子培养基包括:葡萄糖60-80g/L,硫酸镁0.5-1.5g/L,磷酸二氢钾0.5- 1.5g/L,硫酸铵10-15g/L,玉米浆水解液1-1.5g/L,毛发水解液1-1.5g/L,甜菜糖蜜10-15ml/L,苏氨酸0.4-0.6g/L,蛋氨酸0.4-0.6g/L,醋酸盐1-3g/L。 5.根据权利要求1或2所述的发酵方法,其特征在于,所述赖氨酸发酵培养基包括:葡萄糖20-40g/L,硫酸镁0.5-1.5g/L,磷酸0.3-0.5ml/L,硫酸铵9- 14g/L,玉米浆水解液0.5-1g/L,毛发水解液0.5-1g/L,甜菜糖蜜10-15ml/L,甜菜碱0.5-0.8g/L,醋酸盐1-3g/L。 6.根据权利要求2所述的发酵方法,其特征在于,步骤(3)流加葡萄糖溶液和硫酸铵溶液的方法为:发酵培养过程中每2-4h取样测发酵液的还原糖浓 度和氨氮浓度,当发酵液中的还原糖浓度下降至4-8g/L时,开始流加质量体积浓度为50-60%葡萄糖溶液并维持发酵液的还原糖浓度为4-8g/L,当 发酵液中的氨氮浓度下降为1-2g/L时,开始流加质量体积浓度为40-45%硫酸铵溶液并维持发酵液中的氨氮浓度为1-3g/L。 7.根据权利要求6所述的发酵方法,其特征在于,流加质量体积浓度为40%的硫酸铵溶液。 8.根据权利要求2所述的发酵方法,其特征在于,步骤(1)赖氨酸摇瓶种子的接种量为赖氨酸一级培养基体积的1-3‰,培养过程中控制溶氧30%- 50%。 9.根据权利要求2所述的发酵方法,其特征在于,步骤(2)成熟赖氨酸一级种子液的接种量为赖氨酸二级培养基体积的2-5%,培养过程中控制溶氧 30%-50%。 10.根据权利要求2所述的发酵方法,其特征在于,步骤(3)成熟赖氨酸二级种子液的接种量为赖氨酸发酵培养基体积的10-15%,培养过程中控制溶 氧25%-40%。 技术说明书 一种L-赖氨酸的发酵方法 技术领域 本技术属于微生物发酵领域,具体地说,涉及一种发酵生产L-赖氨酸的方法。 背景技术 L-赖氨酸为碱性必需氨基酸,同时也是人体和动物所不能合成的八种必需氨基酸中最重要的一种,故常称为第一限制性氨基酸。人体必需通过日常饮食和补赖氨酸含量甚低,且在加工过程中易被破坏,造成赖氨酸缺乏。 L-赖氨酸在医药工业、食品工业、畜牧饲料等领域都有着广泛的应用。在谷类为主的食品中添加一定量的L-赖氨酸,可提高其蛋白质的吸收率和营养价值;在高饲料的利用率;在医药工业上,L-赖氨酸一般被用作氨基酸输液,可以作为治疗铅中毒的药物、利尿的辅助治疗剂、血栓预防剂。
聚赖氨酸盐酸盐检验方法
检验方法 A.1 安全警示 试验方法规定的一些试验过程可能导致危险情况。操作者应采取适当的安全 和防护措施。 A.2 一般规定 本标准所用试剂和水,在没有注明其他要求时,均指分析纯试剂和GB/T 6682 中规定的三级水。试验中所用标准滴定溶液、杂质测定用标准溶液、制剂及制品,在没有注明其他要求时,均按GB/T 601、GB/T 602、GB/T 603 的规定制备。试验中所用溶液在未注明用何种溶剂配制时,均指水溶液。 A.3 鉴别试验 A.3.1 试剂和材料 A.3.1.1 碱性硝酸铋溶液:碱性硝酸铋0.85 g 加乙酸10 mL 及水40 mL 溶解。A.3.1.2 碘化钾溶液:碘化钾8 g 加水20 mL 溶解。 A.3.1.3 Dragendorf 试液:碱性硝酸铋溶液5 mL、碘化钾溶液5 mL、乙酸20 mL 和水100 mL 混合而成。现用现配。 A.3.1.4 pH 6.8 的0.1 mol/L 磷酸缓冲溶液。 A.3.1.5 甲基橙试液:0.1 mmol/L。 A.3.1.6 正丁醇/水/冰乙酸溶液:(4:2:1)。 A.3.1.7 茚三酮的丙酮溶液:1→50。 A.3.2 分析方法 A.3.2.1 0.1%试样液1 mL 加Dragendorf 试液1 mL,应产生红褐色沉淀。 A.3.2.2 取试样0.1 g 溶于pH6.8 的0.1 mol/L 磷酸缓冲溶液100 mL 中,取试样溶 液1 mL,加甲基橙试液1 mL,应产生红褐色沉淀。 A.3.2.3 参照GB/T5009.124 方法将试样水解成单一氨基酸,制成含本品约1 mg/mL 的近中性水溶液,作为试样溶液;精密称取赖氨酸盐酸盐标准样品适量,加水稀释成1 mg/mL 的溶液,作为标准溶液;另取试样适量,制成含试样约1 mg/mL 的水溶液,作为对照液;另取赖氨酸盐酸盐标准样品与精氨酸标准样品各适量,置于同一量瓶中,用水溶解并稀释成0.4 mg/mL 的溶液,作为系统适用性试验溶液。按照薄层色谱法(《中国药典》附录V B)试验,吸取上述四种溶液各2 μL,分别点于同一硅胶G 薄层板上,以正丁醇/水/冰乙酸溶液为展开剂,展开液由原始线上升高于10 cm 处时,晾干,90 ℃干燥10 min,喷以茚三酮的丙酮溶液,90 ℃ 加热至斑点出现,立即检视。标准溶液应显示一个清晰斑点;系统适应性试验溶液应显示两个完全分离的斑点,且其中一个斑点与标准溶液斑点色泽相似,Rf 值相等;试样溶液所得斑点与标准溶液所示斑点,色泽相似,Rf 值相等。对照液应 在原点处显示一个清晰斑点,没有其它斑点出现。 A.4 ε-聚赖氨酸盐酸盐含量的测定 A.4.1 方法提要 利用高效液相色谱测定ε-聚赖氨酸盐酸盐的含量。 A.4.2 试剂和材料
羟自由基清除率测定
抗氧化活性的测定(参考)——测定活性物质对羟自由基的清除率 (羟自由基清除试验) 采用Fenton 试剂:过氧化氢/亚铁盐。 原理:H 2O 2与亚铁离子反应生成·OH,·OH 自由基一般存活时间比较短,具有较高的反应活性。当在反应体系中添加水杨酸,便能快速的捕捉·OH 而产生紫色化合物(2,3-二羟基苯甲酸),该有色化合物在510nm 处有较大吸收峰,测其吸光度可表示羟自由基(?OH )的多少,吸光度与羟自由基(?OH )的量成正比。反应体系中若加入羟自由基(?OH )清除剂后,被氧化的水杨酸减少,则体系颜色变浅甚至消失,吸光度变小。 操作: 样品处理:蔬菜水果切分,榨汁(切分后可放在2%的盐酸或草酸溶液中护色)。将蔬菜汁或果汁放入50ml 离心管中(如有颜色加适量活性炭或白陶 土),在3000~ 4000rpm 下离心10min~ 20min 后(若样品蛋白含量较高,需加适量乙酸锌,亚铁氰化钾)快速过滤,滤液备用。 取25ml 比色管2支(样品管、空白管),分别加入5ml 1mmol/L 硫酸亚铁溶液、5ml 3mmol/L H2O2溶液,样品管中加入1ml 样品溶液,空白管中加入1ml 蒸馏水,混合均匀后用3mmol/L 水杨酸溶液定容至刻度,在37℃(0.1±℃)的恒温水中反应15min 后,用分光光度计在510nm 的波长下测定各管的吸光度。以3mmol/L 水杨酸溶液调零。 其对?OH 自由基的清除率SA (%),可根据下式进行计算:式中: A0—不加样品的吸光度; A1—加入样品的吸光度 100A0A1-A0= SA(%)?清除率 ###【以往经验,不一定全适用】:若样品不进行脱色处理,则操作如下:在3支25ml 的比色管中(样品管、空白管、样品本底管)依次加入5ml1mmol/L 硫酸亚铁溶液,空白管和样品管中各加入5ml3mmol/L H 2O 2溶液,本底管中H 2O 2溶液用蒸馏水代替。
羟自由基测定试剂盒使用说明
羟自由基测定试剂盒使用说明 货号:LA1950 规格:50管/48样 产品内容: 试剂一:3%H2O2标准品贮备液0.5mL×1支,4℃保存3个月。 0.03%标准品应用液的配置:3%H2O2标准品贮备液:双蒸水=1:99稀释,现用现配。 试剂二:底物贮备液1mL×1支,4℃保存3个月。 底物应用液的配制: 如果您的样本为抑制羟自由基,即测定管吸光度比对照管吸光度低,则底物反应液的配制:底物贮备液:双蒸水=1:99稀释,现用现配。 如果您的样本为产生羟自由基,即测定管吸光度比对照管吸光度高,则底物反应液的配制:底物贮备液:双蒸水=1:299稀释,现用现配。 试剂三:甲液贮备液2mL×1支,4℃保存3个月。用时用双蒸水稀释至1:9稀释成应用液。乙液7mL×2支,4℃保存3个月。 试剂三应用液的配制:甲液应用液与乙液等比列混合,按需配置,剩余的4℃保存。 试剂四:液体10mL×1瓶,4℃保存3个月。用时加双蒸水稀释至100mL制备应用液,4℃保存。若有结晶,则放置37℃水浴至全部溶解后再稀释。 试剂五:液体30mL×1瓶,避光4℃保存3个月。 试剂六:液体30mL×1瓶,避光4℃保存3个月。 试剂七:分析纯的冰乙酸自备。 显色剂的配制:试剂四应用液:试剂五:试剂六:冰乙酸=8:3:3:2,现用现配。 抑制羟自由基的物质如:血清(浆)、各种组织匀浆液、口服液等
产生羟自由基的物质如:中性白细胞、某些药物、部分植物等。 产品简介: Fenton反应是最常见的产生羟自由基的化学反应,H2O2的量和Fenton反应产生的OH·量成正比,当给予电子受体后,用griess试剂显色,形成红色物质,其呈色与OH·的多少成正比列关系。 操作步骤: 以上配制好的应用液,先在37℃水浴中温育3min,一下操作在37℃水浴中进行。 空白管标准管对照管测定管 双蒸水(mL)0.40.20.2 0.03%H2O2标准应用液(mL)0.2 底物应用液(mL)0.20.2 样本(mL)0.2 试剂三应用液(mL)0.40.40.40.4 混匀,37℃反应1min(准确以秒表计时),从加完试剂三开始到1min结束,立即加入显色剂终止反应,一次只能做一个管子。 显色剂2222 混匀,室温放置20min,波长550nm,1cm光径,双蒸水调零,测定各管吸光度值。 参考取样量:血清(浆)样本用生理盐水20倍稀释后取0.2mL做检测;如果您有精确微量移液器,可直接取0.010mL血清(浆),再加0.190mL生理盐水。组织匀浆上清,取0.2mL 检测。具体取样量根据您自己做的预实验确定。 计算:
赖氨酸的生产工艺
1TPM赖氨酸分离提取工艺设计 学生姓名: 学号: 指导教师: 专业名称:生物工程 完成时间: 2011年11月
目录 目录 (1) 第一章项目总论 (3) 1.1赖氨酸的简介 (3) 1.2赖氨酸的性质 (3) 1.3赖氨酸的作用 (3) 1.4赖氨酸的生产方法 (4) 1.4.1二步发酵法 (4) 1.4.2直接发酵法 (4) 1.5赖氨酸的提取精制 (4) 1.6生物工业下游技术的一般工艺过程 (5) 1.7离子交换原理 (5) 第二章技术方案 (1) 2.1产品方案 (1) 2.2发酵工艺流程示意图 (1) 2.3发酵过程工艺流程 (1) 2.3.1发酵法 (1) 2.3.2发酵液的预处理 (2) 2.3.3赖氨酸的提取 (2) 2.3.4浓缩和结晶 (2) 2.4工艺技术指标及基础数据 (2) 2.4.1主要技术指标如下表: (2) 2.4.2主要原材料质量指标 (3) 2.4.3二级种子培养基 (3) 2.4.4发酵培养基 (3) 2.5赖氨酸发酵车间的物料衡算 (3) 2.6热量衡算 (1) 2.6.1发酵过程中的冷却水耗量计算 (1) 2.6.2发酵过程中的无菌空气耗用量的计算 (1) 第三章发酵车间设备设计与选型 (1) 3.1发酵罐的选型 (1) 3.1.1发酵罐容积和台数的确定 (1) 3.1.2主要尺寸的计算 (1) 3.1.3发酵罐冷却面积的计算 (1) 3.1.4发酵罐搅拌器的设计 (1) 3.2电机的确定 (1)
3.2.1 计算Re m (1) 3.2.2计算不通气时的搅拌轴功率P O (1) 3.2.3计算通风时的轴功率Pg (1) 3.2.4求电机功率P电 (1) 3.3发酵罐设备结构的工艺设计 (1) 3.3.1空气分布器 (1) 3.3.2档板 (1) 3.3.3密封方式 (1) 3.3.4 冷却管布置 (1) 3.3.5发酵罐设备材料的选择 (1) 3.4种子罐的选型 (1) 3.4.1种子罐容积和数量的确定 (1) 3.4.2种子罐主要尺寸确定 (1) 3.4.3种子罐型号确定 (1) 3.5赖氨酸提取的树脂设计 (1) 第四章防污措施 (1) 4.1废水的处理 (1) 4.3废渣的处理 (1) 第五章结语 (1) 参考文献 (1)
赖氨酸的品质判断.
赖氨酸的品质判断 1、理化特性 ▲.真赖氨酸为白色或淡褐色小颗粒或粉末。 ▲.真赖氨酸无味或微有异性酸味,假冒赖氨酸气味不正,有些带有芳香性。2、质量指标 表1.饲料级L-赖氨酸盐酸盐质量标准(NY39-1987) 3、主要检测指标及检测方法 ▲.感官检测法:纯品赖氨酸添加剂为白色或淡褐色小颗粒或粉末,无味 或微有特异气味,放入口中带有酸味,口无涩感;假赖氨酸气味不正,具有杂质样涩感,有些还有芳香气味。 ▲.简易检测法:市场流通中不断有伪劣赖氨酸出现,而且做假形式多种 多样,如用淀粉、石粉、石膏粉等冒充或在赖氨酸中掺入这类物质。所以,在没有氨基酸自动分析仪的条件下,如何快速识别赖氨酸的真假很有必 要,现介绍几种快速识别赖氨酸真假的方法: ▲.溶解性检验:赖氨酸易溶于水,难溶于乙醇、乙醚。称取1g赖氨酸样品放入烧杯中,加入50毫升左右的蒸馏水,轻轻搅拌,真赖氨酸溶解完 全,溶液澄清无沉淀物。若溶解不完全,溶液浑浊或有沉淀残渣,则是假冒或掺假赖氨酸。将烧杯再放在电炉上加热,若溶液变稠成糊状,说明样品为以淀粉类物质冒充或掺有淀粉类物质的伪劣赖氨酸。
▲.灼烧法:取1g左右赖氨酸样品放入瓷质坩埚中,在电炉上灼烧,真赖氨酸灼烧时会散发出有类似燃烧羽毛时产生的难闻气味;而假赖氨酸一般不具有这种气味,或气味较淡。当灼烧至无烟后,再移入高温炉中,550℃灼烧2-3小时左右,真赖氨酸的灼烧残渣应在0.3%以下,肉眼几乎看不见残渣。若残渣较多,则为伪劣蛋氨酸,可按根据有关方法进一步鉴别是什么掺假物。 4、判定关键点和注意事项 ▲.定性鉴别L-赖氨酸盐酸盐:L-赖氨酸盐酸盐样品水溶液中加入硝酸银溶液应产生不溶于稀硝酸,而溶于氨水的白色沉淀。 ▲.(1:9)的硝酸溶液配制:1份体积的浓硝酸与9份体积的蒸馏水混合。 ▲.(1:2)的氨水配制:1份体积的浓氨水加2份体积的蒸馏水。 ▲.鉴别方法:称取样品1g,溶于蒸馏水中,加入0.1M硝酸溶液即产生白色沉淀。取此沉淀加(1:9)的硝酸溶液,沉淀不溶解;另取此沉淀,加入过量(1:2)的氨水则溶解。 ▲.可以根据含氮量识别赖氨酸的真伪和估测赖氨酸的含量 赖氨酸分子结构中均含有氮,用饲料常规检验法中粗蛋白质的测定方法,测出其中的含氮量,根据含氮量的多少或有无可判断赖氨酸的真假,估测赖氨酸的含量。 具体方法与粗蛋白的测定方法一样。称取一定量的样品,经消化、蒸馏、接收、盐酸滴定后得出标准盐酸消耗的量,然后按以下公式计算该赖氨酸的含氮量。 N(%)=100×(V-V0)C×0.014×V1/(W×V2)
盐酸赖氨酸精制工艺规程(08)
某制药有限公司 类别:技术标准编号:SP-MF-002-501-01 盐酸赖氨酸精制生产工艺规程版次:?新订?替代: 起草部门:年月日 生产部审核:年月日 技术部审核:年月日 质量部审核:年月日授权:现授权下列部门拥有并执行本标准(复印份) 部门: 批准人: 年月日 生效日期:年月日
目录 1.产品概述 2. 生产操作要求 3.生产处方、处方依据及操作要点 4.原辅料质量标准、技术参数、贮存注意事项 5.生产操作过程 6. 盐酸赖氨酸质量控制要点及成品、中间体质量标准及贮存注意事项 7.设备一览表及主要设备生产能力 8.技术经济指标的计算、消耗定额和经济指标 9.技术安全、劳动保护及防火 10.工艺卫生 11.劳动组织与岗位定员 12.培训
1.产品概述 通用名称:盐酸赖氨酸 英文名称:Lysine Hydrochloride 汉语拼音: Yansuan Laiansuan 化学名称:L-2,6-二氨基己酸盐酸盐。 结构式: H2 , HCl 分子式:C6H14 N2O2·HCl 分子量:182.65
2.生产操作要求 2.1 盐酸赖氨酸生产工艺流程图及工艺监控点 盐酸赖氨酸精制生产工艺规程
2.2生产区域洁净级别划分 图例: 非无菌万级区 无菌万级区 ※ 局部百级区
2.3操作间的位置、洁净度洁别、温湿度要求 3.生产处方 盐酸赖氨酸50Kg 注射用水62.5 Kg 乙醇250 Kg 药用炭0.156 Kg 4、盐酸赖氨酸精制生产工艺过程 4.1盐酸赖氨酸的配滤 4.1.1根据生产指令领盐酸赖氨酸(非无菌粉)、乙醇、活性炭。 4.1.2检查反应罐是否洁净,搅拌、温度计工作是否正常,罐底阀门是否关闭严密,加热供应系统是否正常。 4.1.3按配滤指令打开反应罐加料口,将盐酸赖氨酸、注射用水按重量比为1:1.25加入反应罐,预留5-10kg注射用水。 4.1.4开启反应罐搅拌器,搅拌速度控制为40-50转/min。 4.1.5打开反应罐蒸汽阀,开始加热,溶解控温70±2℃,搅拌60分钟。 4.1.6用预留的5-10kg注射用水,将活性炭润湿,再加入反应罐,搅拌脱色30min。 4.1.7待结晶岗位通知准备好,配滤岗位再关闭反应罐蒸汽阀、搅拌器,趁热
羟自由基清除率测定
抗氧化活性的测定(参考)——测定活性物质对羟自由基的清除率 (羟自由基清除试验) 采用Fenton 试剂:过氧化氢/亚铁盐。 原理:H 2O 2与亚铁离子反应生成·OH,·OH 自由基一般存活时间比较短,具有较高的反应活性。当在反应体系中添加水杨酸,便能快速的捕捉·OH 而产生紫色化合物(2,3-二羟基苯甲酸),该有色化合物在510nm 处有较大吸收峰,测其吸光度可表示羟自由基(?OH )的多少,吸光度与羟自由基(?OH )的量成正比。反应体系中若加入羟自由基(?OH )清除剂后,被氧化的水杨酸减少,则体系颜色变浅甚至消失,吸光度变小。 操作: 样品处理:蔬菜水果切分,榨汁(切分后可放在2%的盐酸或草酸溶液中护色)。将蔬菜汁或果汁放入50ml 离心管中(如有颜色加适量活性炭或白陶土),在3000~ 4000rpm 下离心10min~ 20min 后(若样品蛋白含量较高,需加适量乙酸锌,亚铁氰化钾)快速过滤,滤液备用。 取25ml 比色管2支(样品管、空白管),分别加入5ml 1mmol/L 硫酸亚铁溶液、5ml 3mmol/L H2O2溶液,样品管中加入1ml 样品溶液,空白管中加入1ml 蒸馏水,混合均匀后用3mmol/L 水杨酸溶液定容至刻度,在37℃(0.1±℃)的恒温水中反应15min 后,用分光光度计在510nm 的波长下测定各管的吸光度。以3mmol/L 水杨酸溶液调零。 其对?OH 自由基的清除率SA (%),可根据下式进行计算:式中: A0—不加样品的吸光度; A1—加入样品的吸光度 ###【以往经验,不一定全适用】:若样品不进行脱色处理,则操作如下:在3支25ml 的比色管中(样品管、空白管、样品本底管)依次加入5ml1mmol/L 硫酸亚铁溶液,空白管和样品管中各加入5ml3mmol/L H 2O 2溶液,本底管中H 2O 2溶液用蒸馏水代替。 本底管和样品管分别加入1ml 样品溶液,空白管中加入1ml 蒸馏水,混合均匀后用3mmol/L 水杨酸溶液定容至刻度。在37℃(0.1±℃)的恒温水中反应15min 100A0A1-A0= SA(%)?清除率
赖氨酸含量高的食物有哪些
赖氨酸含量高的食物有哪些 对于人的身体中的所需的元素是很多的,最多的摄入来源就是通过日常的饮食。而生活中的食物都是各种有着独特的功效的,其中就有身体所需的赖氨酸就是通过一些食物摄取的。很多的人可能会因为身体缺赖氨酸出现症状,这个时候就有很多的人想了解下在日常生活中赖氨酸含量高的食物有哪些? 赖氨酸:一般富有蛋白质的食物都含有赖氨酸,如肉类、乳制品和豆类。 黄豆、山药、银杏、大枣、芝麻、蜂蜜、葡萄、莲子,含的赖氨酸比较多。 赖氨酸为碱性必需氨基酸。由于谷物食品中的赖氨酸含量甚低,且在加工过程中易被破坏而缺乏,故称为第一限制性氨基酸。医学|教育|网搜集整理 赖氨酸可以调节人体代谢平衡。赖氨酸为合成肉碱提供结构组分,而肉碱会促使细胞中脂肪酸的合成。往食物中添加少量的赖氨酸,可以刺激胃蛋白酶与胃酸的分泌,提高胃液分泌功效,
起到增进食欲、促进幼儿生长与发育的作用。赖氨酸还能提高钙(补钙产品,补钙资讯)的吸收及其在体内的积累,加速骨骼生长。如缺乏赖氨酸,会造成胃液分沁不足而出现厌食、营养性贫血,致使中枢神经受阻、发育不良。 赖氨酸在医药上还可作为利尿剂的辅助药物,治疗因血中氯化物减少而引起的铅中毒现象,还可与酸性药物(如水杨酸等)生成盐来减轻不良反应,与蛋氨酸合用则可抑制重症高血压病。 单纯性疱疹病毒是引起唇疱疹、热病性疱疹与生殖器疱疹的原因,而其近属带状疱疹病毒是水痘、带状疱疹和传染性单核细胞增生症的致病者。印第安波波利斯Lilly研究室在1979年发 表的研究表明,补充赖氨酸能加速疱疹感染的康复并抑制其复发。 长期服用赖氨酸可拮抗另一个氨基酸――精氨酸,而精氨酸能促进疱疹病毒的生长。 综上所述,大家应也是知道了对于生活中来说赖氨酸含量高的食物最多的就是一些豆制品,同样的就是含蛋白质比较高的食物。同样的对于赖氨酸大家也是可以通过上文中了解下,对于身
STP-QY-122盐酸赖氨酸质量标准及检验规程
目的:明确盐酸赖氨酸的质量标准和规范盐酸赖氨酸的检验规程。 适用范围:盐酸赖氨酸的检验。 责任人:化验员。 引用标准:CP2000版二部。 本品为L-2,6-二氨基已酸盐酸盐。按干燥品计算,含C6H14N2O2不得少于98.5%。 [性状] 本品为白色结晶或结晶性粉末;无臭。 本品在水中易溶,在乙醇中极微溶解,在乙醚中几乎不溶。 比旋度取本品,精密称定,加6mol/L盐酸溶液溶解并稀释成每1ml中含80mg的溶液,依法测定,比旋度为+20.0°至+21.5°。 [鉴别] (1)本品的红外光吸收图谱与对照的图谱(光谱集165图一致)。 (2)本品的水溶液显氯化物的鉴别反应。 [检查] 酸度取本品0.10g,加水10ml溶解后,依法测定,PH值应为5.0—6.0。 溶液的透光度取本品0.5g,加水10ml溶解后,照分光光度法,在430nm 的波长处测定透光率,不得低于98.0%。 硫酸盐取本品1.0g,依法检查,与标准硫酸钾溶液2.0ml制成的对照液比较,不得更浓(0.02%)。 铵盐取本品0.10g,依法检查,与标准氯化铵溶液2.0ml制成的对照液比较,不得更深(0.02%)。 其他氨基酸取本品,加水制成每1ml中含16mg的溶液,作为供试品溶液;精密量取上述溶液适量,加水稀释成每1ml中含80μg的溶液,作为对照溶液。照薄层色谱法试验,吸取上述两种溶解各5μl,分别点于同一硅胶G薄层板上,以正丙醇-氨溶液(2:1)为展开剂,展开后,晾干,在100℃干燥10分钟,喷以茚三酮的丙酮溶液(1→50),在80℃干燥5分钟,立即检视,供试品溶液所显杂质斑点的颜色,与对照溶液的主斑点比较,不得更深(0.5%)。 干燥失重取本品,在105℃干燥3小时,减失重量不得过0.4%。
含赖氨酸多的食物
含赖氨酸多的食物 鳝鱼、泥鳅、鱿鱼、 带鱼、鳗鱼、海参、 墨鱼、蜗牛, 其次有、银杏、 冻豆腐、豆腐皮 山药、鳝鱼、银杏、海参、冻豆腐、海水鱼、豆腐皮、花生、核桃、芝麻等赖氨酸是构成蛋白质的一种必需,而且是不能自己合成,只能从食物中获得的8种必需之一。 含赖氨酸高的食物有:鳝鱼、泥鳅、鱿鱼、带鱼、鳗鱼、海参、墨鱼、蜗牛,其次有、银杏、冻豆腐、豆腐皮。 谷类食物中赖氨酸的含量比较低,如100克大米中含赖氨酸295毫克,100克面粉中含赖氨酸277毫克,仅相当于100克牛肉中赖氨酸含量的1/5,或者100克大豆中赖氨酸含量的1/10。 但现在应用新的生物技术,已研制出了高赖氨酸的玉米等作物。 赖氨酸是人体无法自行生产的必需,因此必须从膳食中摄取。赖氨酸对人体具有多种功能,因为它是许多蛋白质所需的组成部分,而这些蛋白质则为人体多种功能运作所需。并没有特定的RDA限制. 一般上富有蛋白质的食物都含有赖氨酸,如肉类、乳制品和豆类。然而,谷类食品或花生并不含有现成的、人体需要的赖氨酸。 烹煮、烘烤以及过度冷冻,将造成食物中的赖氨酸流失。这也是为什么人体需要辅助品。 通常,素食者(尤指不食用蛋类和乳制品者)较易缺乏赖氨酸。一些从事激烈运动的运动员,对于必需的需求也比常人高。 赖氨酸对于骨骼疏松症具有预防和治疗的作用。增强免疫能力。 黄豆!
赖氨酸是蛋白质的组成成分,一般上富有蛋白质的食物都含有赖氨酸,如肉类、乳制品和豆类。然而,谷类食品或花生并不含有现成的、人体需要的赖氨酸。此外,、银杏、大枣、芝麻、蜂蜜、葡萄、,含的赖氨酸也比较多。富含VB1的食物主要有粮谷类、豆类、干果(如花生)、酵母、坚果类等,动物内脏(肝、肾、心)及瘦肉、蛋类中含量也较丰富,蔬菜较水果含VB1稍多,但不是膳食VB1的主要来源。不过芹菜叶及莴苣叶含量较为丰富,可以利用。 赖氨酸是蛋白质的组成成分,一般上富有蛋白质的食物都含有赖氨酸,如肉类、乳制品和豆类。然而,谷类食品或花生并不含有现成的、人体需要的赖氨酸。此外,山药、银杏、大枣、芝麻、蜂蜜、葡萄、莲子,含的赖氨酸也比较多。富含VB1的食物主要有粮谷类、豆类、干果(如花生)、酵母、坚果类等,动物内脏(肝、肾、心)及瘦肉、蛋类中含量也较丰富,蔬菜较水果含VB1稍多,但不是膳食VB1的主要来源。不过芹菜叶及莴苣叶含量较为丰富,可以利用。 红薯:含有丰富的赖氨酸 红薯今年终于占据了蔬菜榜的头名位置。专家解释说,这是因为红薯中含有丰富的赖氨酸,可以迅速增加饱腹感。而赖氨酸是人体必需氨基酸之一,能促进人体发育、增强免疫功能,并有提高中枢神经组织功能的作用。 《本草纲目》、《本草纲目拾遗》等古代文献均有对红薯功效的记载,中医一般认为红薯有“补虚乏,益气力,健脾胃,强肾阴”的功效。从现代营养学的角度看,红薯中富含的赖氨酸为碱性必需氨基酸。这种物质在谷物食品中一般含量甚低,且在加工过程中易被破坏而缺乏,故称为第一限制性氨基酸。 适当补充赖氨酸能够促进孩子的生长发育,而长期缺少赖氨酸则会使孩子生长停滞、面色苍白、皮肤干燥、肌肉松弛、抵抗力降低,严重的还会影响智力发育。需要提醒大家的是,由于赖氨酸很容易溶解在水中,因此加工红薯时应避免长时间浸泡。此外,赖氨酸不耐高温,故食用红薯时最好以蒸、煮、炖为好。所以,从这个角度说,薯条、薯片多吃也是无益的。 日本国家癌症研究中心最近公布的20种抗癌蔬菜“排行榜”中,红薯也名列榜首。美国费城医院也从红薯中提取出一种活性物质——去雄酮,能有效地抑制结肠癌和乳腺癌的发生。
