间接法Elisa汇总

间接法ELISA SOP
一、包被
1.抗原包被量为20μg/板。
2.例如:抗原浓度为0.8mg/ml。
3.取25μl抗原与20mlCBS(抗原包被液)混匀,100μl/孔。
4.包被完毕后,4℃过夜。
二、封闭
1.从4℃冰箱中取出酶标板,甩干包被液,拍板。
2.加封闭液,200μl/孔。
3.37℃孵育2h。
4.甩干,洗板(3次)。
5.用干燥的自封袋4℃保存。
【注】:洗板,将孔内液体甩出,每孔加200μl -300μl洗板液,静置2min,甩出,将板拍在干的纱布上,将孔内液体拍干为佳。
三、一抗
1.可洗板一次。
2.阳性对照:1μl阳性血清加入1ml抗原稀释液中,做1:1000稀释(第一孔)。
3.阴性对照:做1:2万稀释。
用1μl阴性血清加入100μl抗原稀释液中,先做1:100稀释。再从此液
取出5μl加入995μl的抗原稀释液中,最终稀释为1:2万。
4.空白对照:只加抗原稀释液。
5.除第一孔和阴性对照孔外,每孔加100μl抗原稀释液。
6.第一孔加100μl(1:1000)的阳性对照。
7.第二孔加100μl(1:1000)的阳性对照,吹打混匀,再从二号孔中吸取100μl加到3号孔中,做倍比稀释,最后两孔为阴性对照或空白对照。
1:1000
1:2000
1:4000
1:8000
1:16000
1:32000
阴性对照(1:2万)
空白对照
8.将酶标板37℃孵育1h,洗板3次。
【注】:①通常在第一次做Elisa时,应该做阴性对照的梯度稀释,从中选择最佳的稀释倍数(一般认为吸光值小于0.1的阴性稀释倍数为易)。
②更为严格的操作是,阳性,阴性,空白的对照空均为双复孔或三复孔。
③在稀释一抗,或者二抗的时候,要算好每次的用量。
四、二抗
本次检测采用二抗为辣根过氧化物酶标记的羊抗兔IgG
1.用0.01MPBS做1:5000稀释(现用现配)。
2.100μl/孔。
3.酶标板37℃孵育30min, 洗板3次。
【注】:采用的二抗的所抗的物种应当与一抗的来源相一致,例如一抗是兔多抗,那么二抗就应该选择羊抗兔或者是其他种属抗兔的酶标二抗。
五、显色
2.100μl/孔。
3.酶标板37℃孵育15min,不洗板,直接加终止液。
【注】:①最后显色阳性、阴性、空白都没有一点颜色,很有可能是二抗或者显色剂出了问题。其次还有可能是包被或封闭出了问题,那最后只能是一抗不能和抗原结合了(可能性较小)。
②最后显色阳性、阴性、空白都有颜色,可能是,(1)阳性的显色结果是非特异结
合;(2)阴性稀释不够,或者本身阴性血清就含有可以和抗原结合的物质(动物的个体差异造成);(3)洗板没洗干净,可以增加洗板次数和时间,提高洗板效果。
③出现“跳孔”即,抗体的吸光值并不是根据稀释梯度逐级递减,可能是在做梯度
稀释的时候出现了失误(一般新手的较易出现这种情况)。
六、终止
终止液为2M的H2SO4。
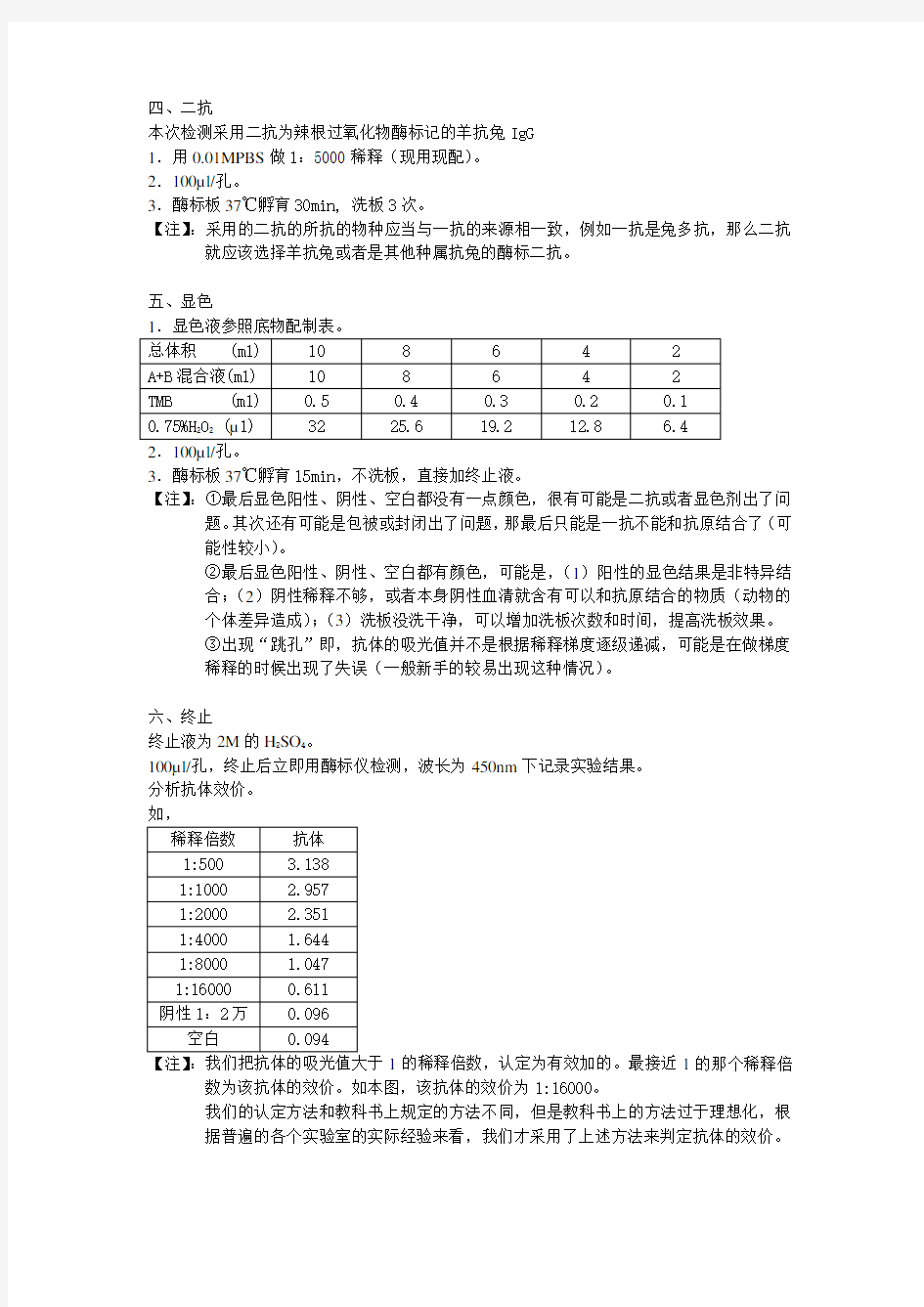
100μl/孔,终止后立即用酶标仪检测,波长为450nm下记录实验结果。
分析抗体效价。
【注】:我们把抗体的吸光值大于1的稀释倍数,认定为有效加的。最接近1的那个稀释倍数为该抗体的效价。如本图,该抗体的效价为1:16000。
我们的认定方法和教科书上规定的方法不同,但是教科书上的方法过于理想化,根据普遍的各个实验室的实际经验来看,我们才采用了上述方法来判定抗体的效价。
附录1 ELISA液配方
包被液【10×CBS】
(pH9.6)配制量1L
配制方法 1.称量下列试剂,置于1L烧杯中。
2.调节pH值至9.6,dH2O定容至1L。
3.4℃保存。
抗原量:200ng/孔,20ug/板。
一抗稀释液(封闭液)配制量100ml
配制方法 1.称量下列试剂。
2.dH2O定容至100ml。
3.注:吐温较为粘稠,用枪吸取时要多停留一会儿。
4.4℃保存。
二抗稀释液【0.01MPBS】
0.1MPBS(PH=7.2) 配制量1L
配制方法 1.称量下列试剂。
2.调节pH值至7.2,dH2O定容至1L。
3.常温保存。
显色液
①A+B混合液配制量50ml
配制方法 1.称量下列试剂。
2.dH2O定容至50ml。
3.4℃保存。
②TMB【四甲基联苯胺】配制量10ml
配制方法 1.称量下列试剂。
2.4℃保存。
③0.75%H2O2配制量400μl
配制方法10μl 30%H2O2+390μl dH2O
注:显色液混合①②③时,现用现混。0.75%H2O2现用现配。
终止液【2M浓H2SO4】配制量1L
配制方法 1.110ml浓H2SO4+890ml dH2O
2.常温保存。
10×洗板液配制量1L
配制方法1L 0.1M PBS+5ml 吐温-20
附录2试剂及仪器厂家
酶标板(96孔)Corning
酶标仪的Thermo
辣根过氧化物酶标记的羊抗兔中杉金桥
附录3 ELISA的基本原理
ELISA的基础是抗原或抗体的固相化及抗原或抗体的酶标记。结合在固相载体表面的抗原或抗体仍保持其免疫学活性,酶标记的抗原或抗体既保留其免疫学活性,又保留酶的活性。在测定时,受检标本(测定其中的抗体或抗原)与固相载体表面的抗原或抗体起反应。用洗涤的方法使固相载体上形成的抗原抗体复合物与液体中的其他物质分开。再加入酶标记的抗原或抗体,也通过反应而结合在固相载体上。此时固相上的酶量与标本中受检物质的量呈一定的比例。加入酶反应的底物后,底物被酶催化成为有色产物,产物的量与标本中受检物质的量直接相关,故可根据呈色的深浅进行定性或定量分析。由于酶的催化效率很高,间接地放大了免疫反应的结果,使测定方法达到很高的敏感度。
原理就是用已知的抗原包被酶标板,经过封闭后,加入待检抗体,再加入抗待检抗体的抗体(抗抗体,即二抗,例如,抗兔免疫球蛋白[IgG]抗体),这个二抗是商品化的,是用一抗做抗原免疫实验动物而制得的,试剂公司都有卖的,往往用碱性磷酸酶(AP)或辣根过氧化物酶(HRP)标记,实验的结果在最后加入该标记酶的底物溶液后通过显色来判断阴性或阳性。抗体结合抗原的位点是Fab端,待检IgG的Fab端就和已知的包被抗原结合,Fc 端游离,加入的二抗就通过其Fab端与IgG的Fc端结合。
分子式CH4N2O 分子量60.06
分子式H2O2,分子量34.01
分子式CO(NH2)2·H2O2 分子量94.07
47%过氧化尿溶液
ELISA显色系统配制试验
显色A液
显色B液
此显色溶液放于4°冰箱中可长期使用。
显色液
①显色缓冲液(A+B混合液)配制量50ml
配制方法 1.称量下列试剂。
2.dH2O定容至50ml。
3.4℃保存。
②TMB【四甲基联苯胺】配制量10ml
配制方法 1.称量下列试剂。
2.4℃保存。
③1.175%过氧化脲配制量400μl
配制方法10μl 47%过氧化脲+390μl dH2O
