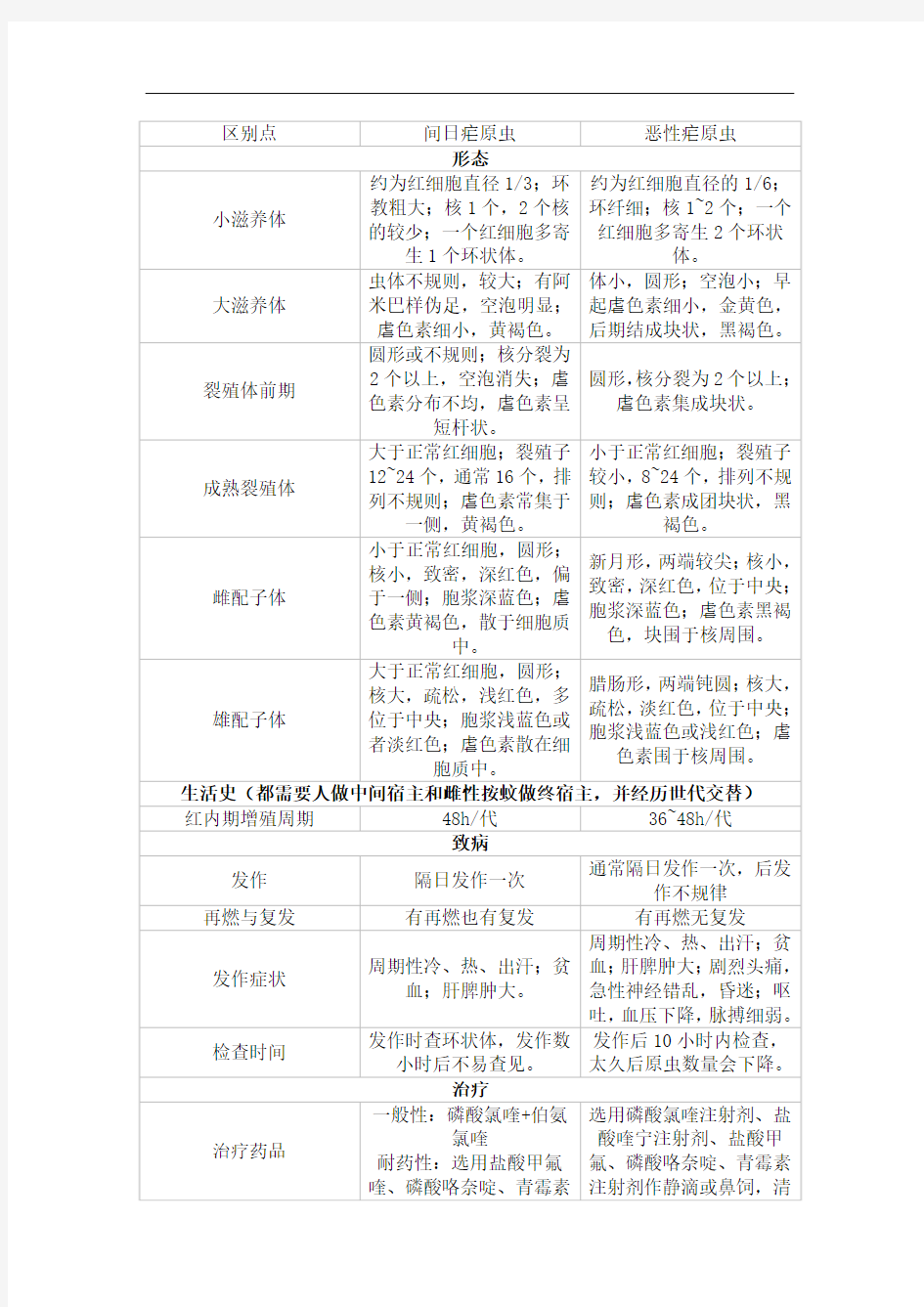
间日疟原虫和恶性疟原虫的区别点

红内期恶性疟原虫转运系统研究进展
第17卷第1期2010年3月 寄生虫与医学昆虫学报 ActaParasit01.Med.Entom01.Sin V01.17,No.1 Mar.,2010 doi:10.3969/j.issn.1005-0507.2010.01.009 红内期恶性疟原虫转运系统研究进展 周洪昌1王恒2’ (1.湖州师范学院医学院微生物与免疫教研室,浙江湖州313000; 2.中国医学科学院基础医学研究所,北京100005) 摘要恶性疟原虫在终末分化的红细胞中发育生长,虽然可以有效的逃避宿主免疫系统的攻击,但同时也面临没有现成的转运系统可供利用等方面的挑战。事实上,红内期疟原虫发展了一套新的转运系统用于其自身蛋白在宿主红细胞中的转运。本文将综述最近几年来红内期恶性疟原虫有关转运信号、蛋白分选和转运等机制方面的最新进展。 关键词恶性疟原虫;蛋白转运 在高等真核生物中,有关蛋白质分泌和内吞等机制已经有详尽的研究。但是对于红内期恶性疟原虫来说,从模式生物研究而来的规律未能完全解释其特有的现象。由于其寄生在终末分化的红细胞内,故面临一些挑战:首先,成熟红细胞中没有细胞器,没有可以直接利用的转运系统;其次,为了生存和繁殖,它需要营养物质的补充和渗透压的平衡。因此,恶性疟原虫不仅需要将蛋白质输送到普通的细胞器,如内质网、高尔基体、线粒体等,还需要将蛋白输送到宿主细胞的胞浆及红细胞膜,以形成新的转运系统。同时,还需要将蛋白输送到如质体、微粒体、棒状体等器官。另外,其营养物质的获取和渗透压的平衡,也需要通过各种途径,摄取周围环境和宿主红细胞中的营养物质(Kirk,2001)。这些转运的有效和正确运作,对于恶性疟原虫来说至关重要。本文将重点介绍最近十多年来恶性疟原虫的分泌和内吞途径两方面的研究进展。 1真核细胞3种经典囊泡转运过程 为更好地了解疟原虫寄生红细胞内的物质转运过程,首先介绍一下真核细胞中经典的转运过程。真核细胞的经典囊泡转运过程的研究已经有超过30年的历史。2004年,《细胞》杂志曾经对该领域的进展做总结性的回顾(Bonifacinoeta1.,2004)。 收稿日期:2009-04—16 ?通讯作者:E-mail:hengwang@puree.edu.cn ?40? 细胞内的转运囊泡不会自发形成,而是一个被高度调控的生物化学过程。在囊泡形成过程中,一系列囊泡蛋白通过程序化的相互作用导致来源膜加囊包被、囊泡形成、脱落、包被蛋白脱落、与靶膜融合、包被蛋白重新循环等一系列有序的过程。COPI和COPII囊泡介导内质网与高尔基体之间的物质转运:COPI主要介导高尔基体到内质网的转运或高尔基囊泡间的转运,COPII主要介导内质网到高尔基体的转运;Clartrin包被的囊泡介导细胞质膜到内体的转运。 2红内期恶性疟原虫的囊泡转运 2.1红内期恶性疟原虫囊泡转运的基础条件2.1.1硬件基础:恶性疟原虫具有其自身的用于囊泡转运的硬件基础。免疫定位技术已经确证了恶性疟原虫的一批内质网的标志蛋白,如分子伴侣PfBip(Kumareta1.,1991),钙结合蛋白PIERC(LaGrecaeta1.,1997),PfSec61的Ot和.y亚基(Couffineta1.,1998)定位在疟原虫胞浆或细胞核周围区域,暗示这些区域可能是恶性疟原虫的内质网或者内质网的一部分。但是,至今只有一些比较零散的证据证明恶性疟原虫中存在高尔基体。恶性疟原虫的高尔基体标志蛋白的同源物如PfERD2(ElmendorfandHaldar,1993)和PfRab6(deCastroeta1.,1996)(顺式和反式高尔基体标志蛋白)是分离存在的,意味着恶
人体疟原虫红内期形态
人体疟原虫红内期形态 涂制于玻片上的红内期疟原虫,经吉氏染色后核呈红色,胞质呈蓝色,疟色素呈黄褐色或深褐色,不着色部分为空泡。 一、薄血膜中疟原虫形态 薄血膜涂制均匀时疟原虫着色良好,结构清晰,便于观察形态和鉴别虫种。薄血膜上各期红内期疟原虫的形态见表1。 表1 薄血膜4种疟原虫形态(吉氏染剂染色) 间日疟原虫恶性疟原虫三日疟原虫卵形疟原虫 被寄生红细胞大小 形状 颜色 斑点 胀大 褪色 薛氏点,红色,细 小数多 正常 正常或稍紫 茂氏点,红色, 粗大数少 正常或缩小 正常 齐氏点淡红色, 微细 正常或稍胀大 卵圆形或边缘呈伞矢状 褪色 薛氏点,粗大数多 早期滋养体(环状体) 大小 核 胞质 色素 较大,约占红细胞 直径的1/3 1个 较薄 无 较小,约占 红细胞直径的1/6 1或2个 纤细 无 中等 1个 较粗厚 偶见细小褐色颗粒 中等 1个 较粗厚 无 大滋养体大小 核 胞质 色素 较大 1个 阿米巴样,常含空泡 黄褐色,细小,杆状, 散在分布 较小 1或2个 圆形,空泡不显著 黄褐色,细小,结成 团块后,呈黑褐色 较小 1个 带状,空泡不显著 深褐色,粗大,沿边 缘分布 较小 1个 圆形,空泡不显著 棕黄色,较粗大 未成熟裂殖体大小 核 胞质 色素 较大 2个以上 圆形或不规则,空泡 消失 黄褐色,分布不匀 较小 2个以上 圆形,空泡消失 黑褐色团块状 较小 2个以上 圆形,空泡消失 深褐色,分布不匀 较小 2个以上 圆形或卵圆形,空泡 消失 棕黄色,分布不匀 成熟裂殖体 大小 裂殖子 色素 大于正常红细胞 12~24个,常为16~18 个,排列不规则,较大 黄褐色,常聚集一侧 小于正常红细胞 8~32个,常为8~18 个,排列不规则,较小 黑褐色团块 小于正常红细胞 6~12个,常为8个, 常排列如菊花状, 较大 深褐色,常聚集中央 小于正常红细胞 6~12个,常为8个, 排列不规则,较大 棕黄色,聚集中央或一 侧
恶性疟原虫基本内容
恶性疟原虫基本内容 恶性疟原虫是寄生在人体内的病原体,有着超强的传染性,不少医院和医学人员对恶性疟原虫进行了研究,可能很多人都不了解恶性疟原虫,也不知道恶性疟原虫的对人体的伤害。被疟原虫感染的人会出现周期性寒战,还会发热,十分不利。恶性疟原虫还会在人体内繁殖,不断的增多。 下面就带大家了解恶性疟原虫。 恶性疟原虫基因组包括大约2400万个碱基对,这些碱基对分布于14条染色体上,编码大约5,300个基因。基因组的分析中,发现了许多寄生虫的代谢途径,例如寄生虫产生能量和自身组成成分以保持生存的途径。疟疾寄生虫的代谢能力比其它自由生活的寄生虫(例如酵母)低很多,它主要依赖于宿主提供生长所需要的大多数营养。然而,在疟原虫中发现了一些酶蛋白,它们在人宿主中没有类似物,这为化学治疗提供了很好的途径。 疟原虫作为一种病原体的成功之处在于它能够逃避人体免疫系统的清除作用。基因组分析过程中发现了大约200种编
码蛋白质的基因,这些蛋白质参与了免疫逃避。以前的研究显示,疟原虫在红细胞中发育的生活史阶段,至少产生了两类暴露于红细胞表面的蛋白质。在某种复杂的掩护机制之下,寄生虫通过在细胞表面表达不同的蛋白质(以此来混淆免疫反应,有助于破坏被感染细胞)来逃避宿主的免疫反应。 编码逃避作用蛋白的多数基因位于染色体的末端。这一位置使寄生虫(在蚊子携带进行繁殖的阶段)易于通过改变编码基因而改变这些蛋白质的结构。基因组序列第一次详细阐明了一种寄生虫的一整套逃避免疫的蛋白质。而且,对于从疟疾病人分离出的其它恶性疟原虫基因组的进一步研究,将发现其它的变种并有助于认识病原体免疫逃避的过程。 疟疾是世界上破坏性最厉害的传染病之一,在发展中国家,每年有超过100万人死于该病。这一成果对于研究治疗疟疾的有效药物和疫苗的研究奠定了坚实的基础。 以上就是恶性疟原虫的相关内容,疟原虫引起的疟疾传染性和破坏性都是很厉害的。所以大家一定要了解疟疾和疟原
恶性疟原虫疫苗的研究进展
恶性疟原虫疫苗的研究进展 发表时间:2015-09-01T10:04:35.823Z 来源:《健康必读》2015年第7期供稿作者:孙红霞亓筱筱冯艺兰(通讯作者)[导读] 成都中医药大学疟疾(Malaria)是全球性严重危害人类健康的重要传染病之一,目前全球有90多个国家和地区的20多亿人居住在疟疾流行区。 孙红霞亓筱筱冯艺兰(通讯作者)(成都中医药大学四川成都610072) 【中图分类号】R531.3【文献标识码】A【文章编号】1672-3783(2015)07-0627-02【摘要】恶性疟原虫是死亡率很高的全球性寄生虫病。由于长期抗疟药的使用,目前恶性疟原虫对主要抗疟药物普遍产生抗药性。(现不少研究和临床观察发现青蒿素类药物的敏感性也逐步下降,提示恶性疟原虫对青蒿素及衍生物的抗药性正在形成。)疫苗的开发及使用成为重要的预防策略,恶性疟原虫疫苗主要有。本文将对恶性疟原虫病原学、流行病学、所致疾病、疫苗研发进展及疫苗使用情况进行综述。 【关键词】恶性疟原虫;疟疾;多期联合疫苗;佐剂 疟疾(Malaria)是全球性严重危害人类健康的重要传染病之一,目前全球有90多个国家和地区的20多亿人居住在疟疾流行区。虽然2010年世界卫生组织报告:疟疾发病案例由2005年2.44亿人次降到2009年2.25亿人次;死亡人数由2000年98.5万例降到2009年的78.1万例,其中非洲地区死亡人数虽然大幅下降,但是目前疟疾仍然是世界六大热带病和我国五大寄生虫病之一,是威胁人类健康的主要疾病,给疫区带来沉重的经济负担,阻碍社会的发展。目前,随着恶性疟原虫抗药株的不断出现已成为重大的公共卫生问题,给疟疾防治工作带来新的挑战,研制有效疫苗已成为预防疟原虫感染的最有效手段。1.病原学及所致疾病疟原虫的基本结构包括核、胞质和胞膜,环状体以后各期尚有消化分解血红蛋白后的最终产物—疟色素。血片经姬氏或瑞氏染液染色后,核呈紫红色,胞质为天蓝至深蓝色,疟色素呈棕黄色、棕褐色或黑褐色。四种人体疟原虫的基本结构相同,但发育各期的形态又各有不同,在滋养体期恶性疟原虫寄生的红细胞有粗大的紫褐色茂氏点(Maurer’sdots)。 疟疾的一次典型发作(parox ysm)表现为寒战、高热和出汗退热三个连续阶段。疟疾数次发作后,易导致贫血和脾肿大,尤以恶性疟为甚。恶性疟原虫可发展为凶险型疟疾,临床表现复杂,常见的有脑型和超高热型,多表现为持续高烧、全身衰竭、意识障碍、呼吸窘迫、多发性惊厥、昏迷、肺水肿、异常出血、黄疸、肾功能衰竭、血红蛋白尿和恶性贫血等。凶险型疟疾来势凶猛,若不能及时治疗,死亡率很高。 在不同疟疾流行区,凶险型疟疾的高发人群和临床表现都很不同。在中度疟疾流行区,脑型疟疾和代谢性酸中毒是儿童常见的凶险型疟疾。在低度疟疾流行区,急性肾衰竭、黄疸和肺水肿是成年人常见的临床表现,贫血、低血糖症和惊厥在儿童中比较多见,而脑型疟疾和代谢性酸中毒在所有的年龄组都可有[1]。 临床诊断主要依据病史、临床症状和实验室检查。目前实验室检测疟原虫的方法主要有血涂片染色镜检法,血清学方法,恶性疟原虫乳酸脱氢酶(LDH.P)电泳法,分子生物学方法.PCR和胶体金免疫层法(GICA)[2]等。现有的诊断方式很难将恶性疟原虫检测出,但是恶性疟起病急,凶险,病情进展快,很容易发展为凶险型疟疾。并且由于耐药性的出现,临床治疗面临困局,预防显得尤为重要。2.流行病学疟疾是严重危害人类健康的疾病之一,有报道,疟疾在全球致死性寄生虫病中位居第一位[3]。在我国以间日疟原虫和恶性疟原虫为主。影响其流行的因素主要有温度、湿度、雨量、地性以及经济水平等。 近年来,面对疟原虫抗药性的不断出现,抗疟药物研究物大的进展,亦无新结构抗疟药问世。因此,疟疾疫苗的研究迫在眉睫。3.疟原虫的免疫应答人体在感染疟疾后诱导产生有效的免疫。此种免疫为种特异性,对异种疟原虫的攻击基本上无保护作用,此外,还有株和期的特异性,人体对疟原虫某一发育期产生的抗性对其他发育期不一定具有抵抗力。 有临床资料显示.IL.27在恶性疟原虫感染的免疫应答过程中起着双向调节作用。与健康婴幼儿血浆相比.非重症疟疾婴幼儿血浆的IL.27的水平较低.重症疟疾婴幼儿血浆IL.27水平在三者中最低。由于疟疾感染中体液免疫与细胞免疫相互调节、相互平衡,多种因素对免疫过程均能产生影响,因此仍有许多问题有待进一步探讨。恶性疟原虫免疫机制研究的不断深入,为疫苗的研制和开发奠定了理论基础。4.恶性疟原虫疫苗的研制进展由于疟原虫与宿主免疫系统的相互作用机制复杂,而物种进化过程中原虫具备了完善的逃逸免疫清除的机制,加之疟原虫抗原具有种、株、期特异性而使抗原分子呈多态。研制由疟原虫多个时期抗原组成的多期联合疫苗是当今疟疾疫苗的发展趋势。 疫苗一直以来是控制传染病的利器,研发特异性高、保护性强的疟疾疫苗已成为有效治理疟疾的权宜之计,而其中的技术关键是能够寻找到免疫原性、反应原性都强且易于高通量表达的疟原虫蛋白。最近研究表明,PfEMPl是体液免疫的关键靶点,但由于编码PfEMPl的var基因家族相互排斥性表达机制存在,因此只有通过常年反复被恶性疟原虫感染,人体的免疫系统才能够识别足够多的PfEMPl,从而缓慢地获得针对恶性疟原虫的免疫保护。 研究证实,佐剂除可增强一些多肽疫苗以及亚单位疫苗的弱免疫原性,不同类型的佐剂还影响抗体亚型、抗体特异性及免疫保护性,不同佐剂所诱导的免疫应答类型也不一致,而特定的免疫应答类型对于某些疾病的保护是至关重要的。对于通过人工多表位串联构建的重组M.RCAg.1蛋白质疫苗,需要在机体内有效呈递所有的表位肽,呈递给B细胞的同时又有效地呈递给T细胞,从而产生高水平的特异性抗体和Th细胞反应。因此,运用于恶性疟原虫疫苗的佐剂还在研究中,需进一步改善。5.存在的问题和展望疟原虫的生活史极为复杂,其先后在人和按蚊两个宿主的5个组织内发生10次形态改变,而每个形态都会有其特异性抗原表达[加之疟原虫抗原具有高度变异性和完善的免疫逃逸系统,以及缺乏高效的佐剂、合适的疫苗递送系统和检测疫苗效力的动物模型,令疟疾疫苗的研制困难重重,以致目前全球尚无被批准使用的疟疾疫苗。但随着免疫学、佐剂以及医学分子生物学的飞速发展,恶性疟原虫疫苗的开发和研制定会很快应用到临床,有效的遏制疟原虫的传播。 参考文献[1]李雍龙.人体寄生虫.第8版.北京:人民卫生出版社,2013:55.62.[2]徐正才,陈芳建,祝进,陈水芳.快速胶体金免疫层析法在恶性疟原虫感染诊断中的应用[J].中国预防学杂志.2013,14(3):233.234.[3]窦晓光,杨绍基,任红.麻疹[M]传染病学.第7版.北京:人民卫生出版社,2008:69.74.
疟原虫形态图谱
原虫形态 期间日疟原虫恶性疟原虫三日疟原虫 环状体胞质淡蓝色,环状,约为 红细胞直径的1/3;核1 个偶有2个;红细胞内 通常寄生1个原虫 环纤细,约为红细胞走 私的1/5,核1-2个,红细 胞内常寄生2个或多个 原虫,虫体位于红细胞 边缘. 与间日疟原虫相似 大滋养 体 核1个,胞质有伪足伸 出,空泡明显,形状不规 则;疟色素棕黄色,细小 杆状分散于胞质内 一般不出现在外周血, 集中于内脏毛细血管, 体小,圆形胞质深蓝,疟 色素黑褐色,块状. 核黄素1个,胞质深蓝, 圆形或带状,疟色素棕 褐色,颗粒状 成熟裂 殖体 虫体充满红细胞,裂殖 子12-24个通常16个, 排列不规则,疟色素集 中成堆 外周血不易见. 裂殖子8-36个,排列不 规则,疟色素集中成一 团 裂殖子较大,6-12个,多 为8个,排列为菊花状, 疟色素集中在中央. 雌配子 体 虫体圆形,胞质深蓝色, 核小,致密,深红色,偏向 一侧,疟色素分散 新月形,两端尖,胞质深 蓝色,核致密深红色位 于中央,疟色素黑褐色 分布核周围 与间日疟相似,虫体较 小 雄配子 体 虫体圆形,胞质蓝,略带 红色,核大疏松,淡红色, 位于中央,疟色素分散 腊肠形,两端印圆,胞质 蓝而略带红色,核疏松 淡红色,位于中央,疟色 素黄棕色分布核周围 与间日疟相似,虫体较 小 被寄生 的红细 胞变化 除环状体外,其余各期 均胀大,色变淡,并有鲜 红色细小数多的薛色 点 正常或略缩小,可有几 颗粗大,紫红色茂氏点 正常或略缩小,颜色无 改变,偶见淡紫色纤细 的西氏点 恶性疟原虫雄配子
恶性疟原虫滋养体 间日疟裂殖体和孢子体 间日疟滋养体 卵圆疟滋养体 三日疟裂殖体和配子体 三日疟滋养体
疟疾多选题
疟疾多选题 三、多选题(每题最少有两个正确答案,多选错选少选和不选均不得分) 1. 疟疾的典型症状有() A. 发热 B. 寒战 C. 呕吐 D. 出汗 E. 咳嗽 2. 下列几种药物中,用于恶性疟治疗的首选药物是() A. 蒿甲醚 B. 双氢青蒿素 C. 青蒿琥酯 D. 氯喹 E. 伯氨喹 3. 疟疾疫点调查与处置内容包括哪些() A. 基本情况 B. 病例筛查 C. 媒介调查控制 D. 健康教育 E. 扩大治疗 4. 寄生于人体的疟原虫主要种类有() A. 间日疟原虫 B. 恶性疟原虫 C. 三日疟原虫 D. 卵形疟原虫 E. 许氏疟原虫 5. 疟疾典型的临床表现各期包括() A. 前驱期B. 寒战期C. 发热期D. 出汗期E. 间歇期 6. 疟原虫在人体内的发育包括() A. 红细胞外期 B. 红细胞内期 C. 配子体形成 D. 子孢子形成 E. 卵囊形成 7. 间日疟外周血涂片中可查见的虫体阶段有() A. 环状体 B. 大滋养体 C. 裂殖体 D. 配子体 E. 子孢子 8. 下列虫体各阶段中,在染色后的血膜上,可查见有疟色素的虫体阶段有() A. 环状体 B. 大滋养体 C. 裂殖体 D. 配子体 E. 以上均可 9. 下列疟原虫种类中,无迟发型子孢子,因而无复发现象的虫种有() A. 恶性疟原虫 B. 间日疟原虫 C. 卵形疟原虫 D. 三日疟原虫 E. 以上都是 10. 制作疟原虫血涂片时,影响血膜染色质量的因素有() A. 染剂和溶剂的质量 B. 染液的新旧 C. 染液的稀释浓度 D. 染色时间 E. 稀释和冲洗用水的酸碱度 11. 涂制均匀染色较好的薄血膜所具有的特点是() A. 疟原虫着色良好 B. 细胞重叠 C. 结构清晰 D. 胞质变形 E. 便于观察疟原虫形态和鉴别虫种 12. 与疟疾传播和流行相关的因素有()
疟原虫形态
形态 发育期 疟原虫在红细胞内生长、发育、繁殖,形态变化很大。一般分为三个主要发育期。 (1)滋养体(trophozoite):为疟原虫在红细胞内摄食和生长、发育的阶段。按发育先后,滋养体有早、晚期之分。早期滋养体胞核小,胞质少,中间有空泡,虫体多呈环状,故又称之为环状体(ring form)。以后虫体长大,胞核亦增大,胞质增多,有时伸出伪足,胞质中开始出现疟色素(malarial pigment)。间日疟原虫和卵形疟原虫寄生的红细胞可以变大、变形,颜色变浅,常有明显的红色薛氏点(Schuffner’s dots);被恶性疟原虫寄生的红细胞有粗大的紫褐色茂氏点(Maurer’s dots);被三日疟原虫寄生的红细胞可有齐氏点(Ziemann’s dots)。此时称为晚期滋养体,亦称大滋养体。 (2)裂殖体(schizont):晚期滋养体发育成熟,核开始分裂后即称为裂殖体。核经反复分裂,最后胞质随之分裂,每一个核都被部分胞质包裹,成为裂殖子(merozoite),早期的裂殖体称为未成熟裂殖体,晚期含有一定数量的裂殖子且疟色素已经集中成团的裂殖体称为成熟裂殖体。 (3)配子体(gametocyte):疟原虫经过数次裂体增殖后,部分裂殖子侵入红细胞中发育长大,核增大而不再分裂,胞质增多而无伪足,最后发育成为圆形、卵圆形或新月形的个体,称为配子体;配子体有雌、雄(或大小)之分:雌(大)配子体虫体较大,胞质致密,疟色素多而粗大,核致密而偏于虫体一侧或居中;雄(小)配子体虫体较小,胞质稀薄,疟色素少而细小,核质疏松、较大、位于虫体中央。 超微结构 (1)裂殖子:红细胞 显微镜下的疟原虫 内期裂殖子呈卵圆形,有表膜复合膜(pellicular complex)包绕。大小随虫种略有不同,平均长1.5µm,平均直径1µm。 表膜(pellicle)由一质膜和两层紧贴的内膜组成。质膜厚约7.5µm,内膜厚约15µm,有膜孔。紧靠内膜的下面是一排起于顶端极环(polar ring)并向后部放散的表膜下微管(subpellicular microtubule)。内膜和表膜下微管可能起细胞骨架作用,使裂殖子有硬度。游离的裂殖子的外膜有一厚约20µm表被(surface coat)覆盖。此表被是电子致密、坚实的纤丝,在性质上似是蛋白质,可能在对宿主免疫反应的应答中起作用。在裂殖子侧面表膜有一胞口(cytostome),红细胞内期各期原虫通过胞口摄取宿主细胞浆。 裂殖子顶端是一截头的圆锥形突起称为顶突(apical prominence),有三个极环。在此区可见两个电子致密的棒状体(rhoptry)和数个微线体(micronemes)。棒状体和微线体可能在裂殖子侵入宿主细胞时起作用。裂殖子后部可见一线粒体。内质网很少,但胞浆内有丰富的核糖体。高尔基氏复合体不明显。裂殖子的核大而圆,位于虫体后半部,沿核膜可见核孔,未见有核仁。 (2)子孢子:子孢子形状细长,长约11µm,直径为1.0µm,常弯曲呈C形或S形,前端稍细,顶端较平,后端钝圆,体表光滑。子孢子内的细胞器基本上与裂殖子相似。表膜由一外膜、双层内膜和一层表膜下微管组成。膜下微管自极环向后延伸至核或稍越过核而终止。虫体的微弱运动可能是膜下微管的伸缩引起的。子孢子的前端顶部有一向内凹入的顶杯(anterior cup)即顶突,在顶突的周围有3~4个极环。细胞核一个,长形。有一对电子致密的棒状体,可能开口于顶环。在核的前方或后方,有数量很多的微线体,呈圆形、卵圆形或长形。[1]
寄生于人体的疟原虫有4种
寄生于人体的疟原虫有4种,由4种不同的疟原虫引起,即:间日疟(vivax malaria,benign tertian),病原为间日疟原虫(Plasmodium vivax);三日疟(quartan malaria,malariae malaria),病原为三日疟原虫(P.malariae);卵形疟(ovale malaria),病原为卵型疟原虫(P.ovale);恶性疟(faleiparuma mlaria,malignant tertian),病原为恶性疟原虫(P.faleiparu-m)。 人感染疟原虫后可产生相当程度的免疫,所以在疟区,当地人由于早年多患过疟疾,均获得相当程度的免疫力。而外地人由于无免疫力,进入全疟区后容易被感染。疟区的婴儿,降生后一个月内,有来自母体的抗体保护;一个月后,疟疾的发病率与死亡率均很高。 1957年泰国发现抗氯喹的疟疾病人。1960年哥伦比亚正式报告了此类患者。[1] 编辑本段发病机制 疟原虫在红细胞中增殖成裂殖子,使红细胞胀大破裂时,大量的裂殖子和疟原虫代谢产物进入血流,引起异性蛋白反应,机体肌肉收缩产热,网状内皮系统吞噬细胞功能增强,故可引起肝、脾肿大,多次发作可致贫血等。疟原虫在红细胞内增殖成熟所需时间不同,间日疟和卵形疟为48小时,三日疟为72小时,恶性疟为24~48小时,故临床上出现周期性发作。 [2] 编辑本段病原学 分类 寄生于人体的疟原虫有4种,即间日疟、恶性疟、三日疟和卵形疟。 形态及生活史 疟原虫生活史比较复杂。一个完整的生活史包括在人体内的生长及繁殖(肝细胞内一红外期,及红细胞内一红内期)及在按蚊体内生长及繁殖两个阶段。4种疟原虫的生活史基本相同。 ⑴疟原虫在人体内发育:[2] ①红细胞外期:按蚊吸人血时唾液中的子孢子随唾液进入人体的末梢血液中,约经30分钟,随血流进入肝脏,在肝内发育,进行裂体增殖,此时期称红细胞外期,简称红外期,亦称肝内期或组织期。红外期裂殖体增殖时间为:间日疟原虫8天,恶性疟原虫5.5~6天,卵形疟9天,三日疟原虫11~12天。当红外期裂殖体发育成熟时,被寄生的肝细胞破裂,裂殖子散出,释放至周围血循环中,一部分被吞噬细胞吞噬,另一部分则侵入红细胞内发育。⑵红细胞内期:红外期裂殖子侵入红细胞便开始在红细胞内进行裂体增殖,该期称红细胞内期,简称红内期。 在红内期,各种疟原虫完成裂体增殖周期所需的时间有所不同。间日疟和卵形疟原虫为48小时,恶性疟原虫为36~48小时,三日疟为72小时。 ⑵在蚊体内发育:雌雄配子体在蚊体内的发育和繁殖包括配子生殖和孢子增殖两个阶段。编辑本段流行病学 1.传染源病人和无症状的血中有配子体的人是疟疾的传染源。 2.传播媒介为按蚊(Anopheles)。按蚊共200种左右,但传疟者并不多,只有吸人血、对疟原虫易感、群体的数量大、生活期较长、子孢子可在其体内发育成熟的蚊种才可成为媒介。而且一种按蚊在甲地起传疟作用,而在乙地则不一定。 3、传播方式绝大多数为,被有传染性的按蚊叮咬后而受染。罕见的情况下经胎盘的先天性感染、输血、麻醉药成瘾的人打麻醉针时针头或注射器消毒不良等均可传染。 4、易感者所有人对4种疟原虫均易感。但黑种人对间日疟敏感性差。原因不明。 人感染疟原虫后可产生相当程度的免疫,所以在疟区,当地人由于早年多患过疟疾,均获得相当程度的免疫力。而外地人由于无免疫力,进入全疟区后,不被感染者极少。 疟区的婴儿,降生后一个月内,由于受来自母体的抗体保护,一个月后,疟疾的发病率与死亡率均很高。 5.影响疟疾流行的因素
疟原虫图谱
约占寄生红细胞的1/3,很少见到一个红细胞寄生2个环状体和一个环状体有2个核。 恶性疟环状体: 环纤细,约为RBC直径的1/6,RBC不胀大 核1个,但2个常见,红细胞常含2个以上原虫
虫体不规则,较大;阿米巴样空泡明显;疟色素细小,黄褐色。 恶性疟大滋养体: 虫体较小,蓝色,圆形,坚实,体积小。 较细的黑褐色颗粒,常集成块。
间日疟成熟裂殖体: 红细胞:胀大,褪色,可见薛氏小点。大小:个体较大。 胞浆和核:裂殖子12~24个,通常为16~18个,排列不规则,核红色,胞浆浅蓝色。疟色素:黄褐色,常集于疟原虫的一边。 恶性疟成熟裂殖体: 红细胞:大小正常,颜色较深,可见茂氏小点。大小:虫体较小。裂殖子8~32个,通常8~18个,排列不规则;疟色素集中成团块状;虫体占红细胞体积的2/3至3/4
间日疟原虫雌配子体: 形状大小:圆形或椭圆形,较大。胞浆:深蓝色。核:一个,较小,深红色,常偏于一边,核周可见明显不染色带。疟色素:黄褐色,均匀散在,数目较多。 间日疟原虫雄配子体: 形状大小:圆形,虫体较大。胞浆:浅蓝色。核:一个,较大,疏松,位于中央,浅红色,周围有明显不着色带。疟色素:黄褐色,散在分布。
恶性疟雌配子体: 形状:新月形,两端稍尖。胞浆:深蓝色。核:一个,较小,致密,深红色,位于中央,核周可见透明不染色带。疟色素:黑褐色,密布于核的周围。 恶性疟雄配子体: 形状:腊肠形,两端钝圆。胞浆:浅蓝色或淡紫红色。核:一个,较大,疏松,位于中央,浅红色,核周可见不染色带。疟色素:黑褐色,松散分布于核周围。
1.红细胞通常胀大; 2.薛氏点明显; 3.成熟环状体粗大; 4.滋养体有阿米巴样伪足; 5.可见不同发育期的原虫 恶性疟鉴定要点: 1.环状体钎细, 红细胞不涨大; 2.一个红细胞内可有几个环状体; 3.环状体内可有2个核; 4.环状体可贴在红细胞边缘; 5.血片中没有其他发育期滋养体 6.配子体呈新月形或腊肠形; 7.可出现茂氏点
疟原虫
编辑 锁定 疟原虫为按蚊传播的孢子虫,是疟疾(malaria)的病原体。寄生于人体的疟原虫有四种,即间日疟原虫(Plasmodium vivax Grassi & Feletti,1890)、三日疟原虫(Plasmodium malariae Laveran,1881)、恶性疟原虫(Plasmodium falciparum Welch,1897)和卵形疟原虫(Plasmodium ovale Stephens,1922)。[1] 这些疟原虫有蚊虫和人两个宿主,包括蚊体内的有性繁殖和人体内的无性增殖,携带疟原虫的按蚊通过叮咬人而传播,引起疟疾寒热往来发作,俗称“打摆子”。而其他种类的疟原虫会感染它种动物,包括其他灵长目动物、啮齿目动物、鸟类及爬虫类。 中文学名 疟原虫属 拉丁学名 Plasmodium 界 原生生物界 门 原生动物门 纲 孢子虫纲 亚纲 晚孢子亚纲 目 真球虫目或血孢子虫目 科 疟原虫科 属 疟原虫属 目录 1 种类 2 形态 ?发育期 ?超微结构 3 生活史 ?在人体内的发育 ?在按蚊体内的发育 4 营养代谢 ?葡萄糖代谢 ?蛋白质代谢 ?核酸代谢 ?脂类代谢 5 致病阶段 ?潜伏期 ?疟疾发作 ?再燃和复发
?脾肿大 ?凶险型疟疾 ?疟性肾病 ?先天性疟疾 ?输血疟疾 6 免疫种类 ?先天抵抗力 ?获得性免疫 7 实验诊断 ?病原学诊断 ?免疫学诊断 ?分子生物学技术 8 流行病学 ?流行概况 ?流行环节 9 防治方法 疟原虫种类 编辑 疟原虫种类繁多,寄生于人类的疟原虫有4种,即恶性疟原虫[Plasmodium falciparum(Welch,1897) Schaudinn,1902]、间日疟原虫[Plasmodium vivax(Grassi and Felletti,1890) Labbe,1899]、三日疟原虫[Plasmodium malariae (Laveran,1881) Grassi and Felletti,1890]和卵形疟原虫[Plasmodium ovale Stephens,1922],分别引起恶性疟、间日疟、三日疟和卵形疟。我国主要感染为恶性和间日疟疾,偶尔有传入性三日和卵形疟疾。 疟原虫的基本结构包括核、胞质和胞膜,环状体以后各期尚有消化分解血红蛋白后的最终产物—疟色素。血片经姬氏或瑞氏染液染色后,核呈紫红色,胞质为天蓝至深蓝色,疟色素呈棕黄色、棕褐色或黑褐色。四种人体疟原虫的基本结构相同,但发育各期的形态又各有不同,可资鉴别。除了疟原虫本身的形态特征不同之外,被寄生的红细胞在形态上也可发生变化。被寄生红细胞的形态有无变化以及变化的特点,对鉴别疟原虫种类很有帮助。[2] 疟原虫形态 编辑 疟原虫发育期 疟原虫在红细胞内生长、发育、繁殖,形态变化很大。一般分为三个主要发育期。 (1)滋养体(trophozoite):为疟原虫在红细胞内摄食和生长、发育的阶段。按发育先后,滋养体有早、晚期之分。早期滋养体胞核小,胞质少,中间有空泡,虫体多呈环状,故又称之为环状体(ring form)。以后虫体长大,胞核亦增大,胞质增多,有时伸出伪足,胞质中开始出现疟色素(malarial pigment)。间日疟原虫和卵形疟原虫寄生的红细胞可以变大、变形,颜色变浅,常有明显的红色薛氏点(Schuffner’s dots);被恶性疟原虫寄生的红细胞有粗大的紫褐色茂氏点(Maurer’s dots);被三日疟原虫寄生的红细胞可有齐氏点(Ziemann’s dots)。此时称为晚期滋养体,亦称大滋养体。 (2)裂殖体(schizont):晚期滋养体发育成熟,核开始分裂后即称为裂殖体。核经反复分裂,最后胞质随之分裂,每一个核都被部分胞质包裹,成为裂殖子(merozoite),早期的裂殖体称为未成熟裂殖体,晚期含有一定数量的裂殖子且疟色素已经集中成团的裂殖体称为成熟裂殖体。
恶性疟原虫
恶性疟原虫 摘要:疟疾是一类在热带和亚热带地区非常流行的疾病,混合感染现象普遍存在。恶性疟原虫与人体细胞相互作用的过程中,子孢子通过黏附肝内皮细胞受体侵入肝脏,裂殖子感染红细胞利用其表面膜蛋白与人体重要器官的血管内皮细胞表面多糖分子发生黏附,最终导致血流受阻。而恶性疟原虫变异抗原基因var 基因家族的相关变异机制使恶性疟原虫的治疗和预防带来极大困难,本文对恶性疟原虫感染机理与其他病原体共染、及其var基因做统一综述 关键词:恶性疟原虫多糖黏附混合感染var基因 疟疾广泛流行于世界各地,是一种不易控制、严重危害人体健康的寄生虫病。尽管目前采取控制措施,但世界上每年恶性疟病例大于5亿,每年约有100万儿童因感染恶性疟死亡。据统计,在重症恶性疟中,脑型疟致死率最高,而幸存的脑型疟儿童有10%会出现不同程度的神经系统损害症状,如偏瘫和失语。由于感染疟原虫后会对机体免疫系统产生破坏,因此居住在疟疾流行区的人们会更容易感染其他的病原体,从而引起其他疾病,最为常见的是疟疾与HIV、EB病毒、疟疾与结核杆菌的混合感染。 1疟原虫感染人体后的发育 分为肝细胞内的发育和红细胞内的发育二个阶段 1.1红细胞外期 当唾腺中带有成熟子孢子的雌性按蚊刺吸人血时,子孢子随唾液进入人体,后随血流侵入肝细胞,摄取肝细胞内营养进行发育并进行裂体增殖,形成红细胞外期裂殖体。成熟的红细胞外期裂殖体内含数以万计的裂殖子。裂殖子胀破肝细胞后释出,一部分裂殖子被巨噬细胞吞噬,其余部分侵入红细胞,开始红细胞内期的发育。而恶性疟原虫无休眠子,使其感染到发病时间更短,给治疗带来了不便。 1.2红细胞内期 红细胞外期的裂殖子从肝细胞释放出来,进入血流后很快侵入红细胞。裂殖子侵入红细胞的过程包括以下步骤 ①裂殖子通过特异部位识别和附着于红细胞膜表面受体 ②红细胞广泛性变形,红细胞膜在环绕裂殖子处凹入形成纳虫空泡 ③裂殖子入侵完成后,纳虫空泡密封。在入侵过程中裂殖子的细胞表被脱落于红细胞中
疟原虫形态
疟原虫形态 四种疟原虫在红细胞内的各期形态不尽相同,是诊断、鉴别各种疟原虫的依据。瑞氏染色或姬氏染色后疟原虫的细胞质呈蓝色,细胞核呈红色,疟色素呈棕褐色。现将薄血片染色后的间日疟原虫各个时期形态(滋养体、裂殖体、配子体)介绍如下: 1.滋养体(trophozoite):是疟原虫在红细胞内摄取营养和发育的阶段。当裂殖子侵入红细胞后,虫体胞质较少,中间出现大空泡,胞质呈环状,细胞核位于虫体一侧,颇似戒指的宝石。因此,早期滋养体又称为环状体(ring form)。环状体继续发育,长大。间日疟原虫和卵形疟原虫约经8~10小时,恶性疟原虫约经10小时,三日疟原虫约经24小时,虫体增大,伸出伪足,为运动细胞器,同时胞质中出现少量疟色素(malarialpigment);随着虫体继续发育,疟色素增多,伪足活动增加,出现多种形态,虫体有1或2~3个空泡。受染的红细胞胀大可达1倍,颜色变淡,并出现能染成淡红色的小点,称薛氏小点(Schhffner,s dots)。恶性疟原虫的早期滋养体在外周血液中经十几小时的发育,逐渐隐匿于各种器官组织的毛细血管中,继续发育成滋养体。 四种人体疟原虫滋养体形态比较(薄片,吉氏液染色) 间日疟原虫恶性疟原虫三日疟原虫卵形疟原虫 小 滋
养体较大,约为红细胞直 径的1/3,环粗大, 核1或2个;红细 胞的多虫感染不多 见 约为红细胞直径的 1/6,环纤细,核1~2 个,有些贴于红细胞边 缘;红细胞的多虫感染 比较常见 约为红细胞直径的 1/3,环教粗,核1个; 红细胞的多虫感染很 少见 似三日疟原虫 大滋 养体较大,阿米巴样,空 泡明显;核较大,疟 色素细小,黄褐色, 短杆状 通常在外周血中看不 到;中等大小,很少呈 阿米巴样。早期疟色素 细小,金黄色,晚期结 成块状,黑褐色 常称带状而非阿米巴 样,空泡小,疟色素较 粗大,深褐色,常沿虫 体边缘分布 常呈圆形或不整圆 形,疟色素粗大,暗 褐色返回标题 2.裂殖体(schizont):约经40小时,间日疟原虫晚期滋养体发育成熟,虫 体变圆,胞质内空泡消失,核开始分裂,称未成熟裂殖体(immature schizont)。之后核继续分裂,胞质随之分裂,疟色素渐趋集中。最后,分裂的每一小部分胞质包绕一个胞核,形成裂殖子。这时含有裂殖子的虫体称为成熟裂殖体。间日疟原虫的成熟裂殖体常充满于被寄生的红细胞,最后形成12~24个裂殖子。裂殖子长约1.5um,宽约1um。在红细胞受染后48小时左右,形成成熟裂殖体。
