限制性内切酶保护碱基

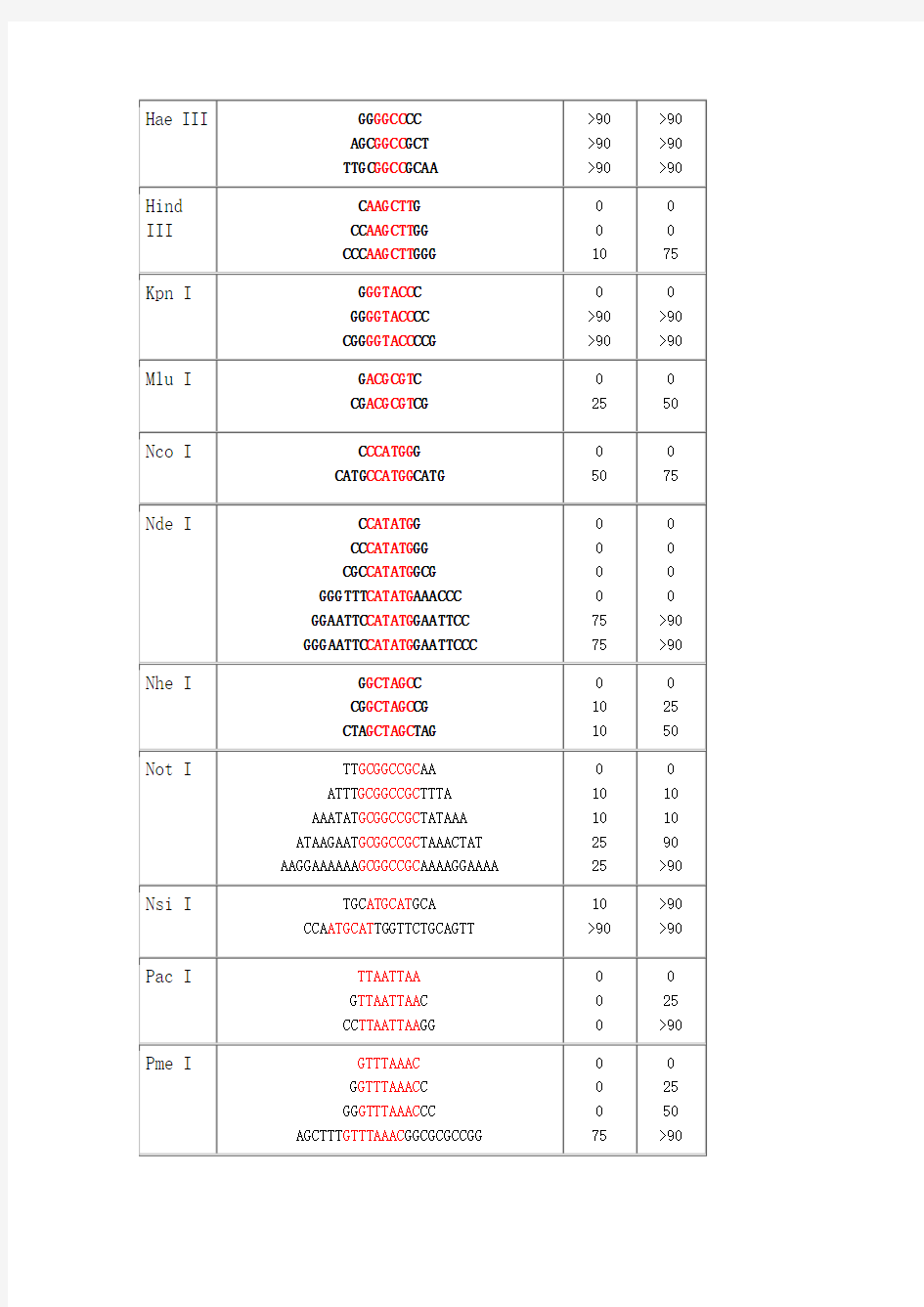
酶切位点保护碱基表
酶切位点保护碱基-PCR引物设计用于限制性内切酶 酶切反应 来源:easylabs 发布时间:2009-11-08 查看次数:12704 本文给出了分子克隆中常用限制性内切酶的保护碱基序列,如AccI,A flIII,AscI,AvaI,BamHI,BglII,BssHII,BstEII,BstXI,ClaI,E coRI,HaeIII,HindIII,KpnI,MluI,NcoI,NdeI,NheI,NotI,N siI,PacI,PmeI,PstI,PvuI,SacI,SacII,SalI,ScaI,SmaI,S peI,SphI,StuI,XbaI,XhoI,XmaI, 为什么要添加保护碱基? 在分子克隆实验中,有时我们会在待扩增的目的基因片段两端加上特定的酶切位点,用于后续的酶切和连接反应。由于直接暴露在末端的酶切位点不容易直接被限制性核酸内切酶切开,因此在设计PCR引物时,人为的在酶切位点序列的5‘端外侧添加额外的碱基序列,即保护碱基,用来提高将来酶切时的活性。 其次,在分子克隆实验中选择载体的酶切位点时,相临的两个酶切位点往往不能同时使用,因为一个位点切割后留下的碱基过少以至于影响旁边的酶切位点切割。 该如何添加保护碱基? 添加保护碱基时,最关心的应该是保护碱基的数目,而不是种类。什么样的酶切位点,添加几个保护碱基,是有数据可以参考的。 添加什么保护碱基,如果严格点,是根据两条引物的Tm值和各引物的碱基分布及GC含量。如果某条引物Tm值偏小,GC%较低,添加时多加G或C,反之亦反。 为了解不同内切酶对识别位点以外最少保护碱基数目的要求,NEB采用了一系列含识别序列的短双链寡核苷酸作为酶切底物进行实验。实验结果对于确定双酶切顺序将会有帮助(比如在多接头上切割位点很接近时),或者当切割位点靠近DNA末端时也很有用。在本表中没有列出的酶,则通常需在识别位点两端至少加上6个保护碱基,以确保酶切反应的进行。 实验方法:用γ-[32P]ATP在T4多聚核苷酸激酶的作用下标记0.1A2 60单位的寡核苷酸。取1μg已标记了的寡核苷酸与20单位的内切酶,在2 0°C条件下分别反应2小时和20小时。反应缓冲液含70mM Tris-HCl (pH 7.6), 10 mM MgCl2, 5 mMDTT及适量的NaCl或KCl(视酶的具体要求而定)。20%的PAGE(7M尿素)凝胶电泳分析,经放射自显影确定酶切百分率。
酶切位点保护碱基
酶寡核苷酸序列 切割率% 2 hr20 hr Not I TT GCGGCCGC AA ATTT GCGGCCGC TTTA AAATAT GCGGCCGC TATAAA ATAAGAAT GCGGCCGC TAAACTAT AAGGAAAAAA GCGGCCGC AAAAGGAAAA 10 10 25 25 10 10 90 >90 Nsi I TGC ATGCAT GCA CCA ATGCAT TGGTTCTGCAGTT 10 >90 >90 >90 Pac I TTAATTAA G TTAATTAA C CC TTAATTAA GG 0 25 >90 Pme I GTTTAAAC G GTTTAAAC C GG GTTTAAAC CC AGCTTT GTTTAAAC GGCGCGCCGG 75 25 50 >90 Pst I G CTGCAG C TGCA CTGCAG TGCA AA CTGCAG AACCAATGCATTGG AAAA CTGCAG CCAATGCATTGGAA CTGCAG AACCAATGCATTGGATGCAT 10 >90 >90 10 >90 >90 Pvu I C CGATCG G AT CGATCG AT TCG CGATCG CGA 10 25 10 Sac I C GAGCTC G1010 Sac II G CCGCGG C TCC CCGCGG GGA 50 >90 Sal I GTCGAC GTCAAAAGGCCATAGCGGCCGC GC GTCGAC GTCTTGGCCATAGCGGCCGCG G ACGC GTCGAC GTCGGCCATAGCGGCCGCG GAA 10 10 50 75 Sca I G AGTACT C AAA AGTACT TTT 10 75 25 75
限制性内切酶保护碱基表
PCR设计引物时酶切位点的保护碱基表
ApaI (类型:Type II restriction enzyme )识别序列:5'GGGCC^C 3' BamHI(类型:Type II restriction enzyme )识别序列:5' G^GATCC 3' BglII (类型:Type II restriction enzyme )识别序列:5' A^GATCT 3' EcoRI (类型:Type II restriction enzyme )识别序列:5' G^AATTC 3' HindIII (类型:Type II restriction enzyme )识别序列:5' A^AGCTT 3' KpnI (类型:Type II restriction enzyme )识别序列:5' GGTAC^C 3' NcoI (类型:Type II restriction enzyme )识别序列:5' C^CATGG 3' NdeI (类型:Type II restriction enzyme )识别序列:5' CA^TATG 3' NheI (类型:Type II restriction enzyme )识别序列:5' G^CTAGC 3' NotI (类型:Type II restriction enzyme )识别序列:5' GC^GGCCGC 3' SacI (类型:Type II restriction enzyme )识别序列:5' GAGCT^C 3' SalI (类型:Type II restriction enzyme )识别序列:5' G^TCGAC 3' SphI (类型:Type II restriction enzyme )识别序列:5' GCATG^C 3'
各种酶切位点的保护碱基引物设计必看
各种酶切位点的保护碱基 酶不同,所需要的酶切位点的保护碱基的数量也不同。一般情况下,在酶切位点以外多出3个碱基即可满足几乎所有限制酶的酶切要求。在资料上查不到的,我们一般都随便加3个碱基做保护。 寡核苷酸近末端位点的酶切 (Cleavage Close to the End of DNA Fragments (oligonucleotides) 为了解不同内切酶对识别位点以外最少保护碱基数目的要求,NEB采用了一系列含识别序列的短双链寡核苷酸作为酶切底物进行实验。实验结果对于确定双酶切顺序将会有帮助(比如在多接头上切割位点很接近时),或者当切割位点靠近DNA末端时也很有用。在本表中没有列出的酶,则通常需在识别位点两端至少加上6个保护碱基,以确保酶切反应的进行。 实验方法:用γ-[32P]ATP在T4多聚核苷酸激酶的作用下标记0.1A260单位的寡核苷酸。取1 μg 已标记了的寡核苷酸与20单位的内切酶,在20°C条件下分别反应2小时和20小时。反应缓冲液含70 mM Tris-HCl (pH , 10 mM MgCl2 , 5 mM DTT及适量的NaCl或KCl(视酶的具体要求而定)。20%的PAGE(7 M尿素)凝胶电泳分析,经放射自显影确定酶切百分率。 本实验采用自连接的寡核苷酸作为对照。若底物有较长的回文结构,切割效率则可能因为出现发夹结构而降低。
2.双酶切的问题 参看目录,选择共同的buffer。其实,双酶切选哪种buffer是实验的结果,takara公司从1979年开始生产限制酶以来,做了大量的基础实验,也积累了很多经验,目录中所推荐的双酶切buffer 完全是依据具体实验结果得到的。 有共同buffer的,通常按照常规的酶切体系,在37℃进行同步酶切。但BamH I在37℃下有时表现出star活性,常用30℃单切。 两个酶切位点相邻或没有共同buffer的,通常单切,即先做一种酶切,乙醇沉淀,再做另一种酶切。 3.酶切底物DNA,切不开 1)底物DNA上没有相应的限制酶识别位点,或酶切位点被甲基化。 2)PCR引物的酶切位点前没有保护碱基或引物合成有误,致使没有正确的酶切位点存在。PCR产物酶切前尽量进行精制以更换buffer。由于PCR产物中带入的其它物质,会影响酶切,据报道,通常PCR产物的添加量占总反应体积25%以下没有问题。 3)酶切条件的确认,包括反应温度和反应体系等。同样的DNA,同样量,用不同的限制酶切情况可能不同,由于DNA的空间结构造成的。同样的DNA,不同的反应体系,酶切效果也可能不同,由于一些空间因素或不可测因素造成的。 4)公司出售的限制酶都是液体状态,都是根据最佳反应体系配制了浓度,不可以再用buffer稀释,因为酶浓度和活性之间不呈直线对应关系,酶浓度越稀,相对活性越低,并且越不稳定,有时便会出现底物DNA不能被切断的现象。 不同公司的酶和buffer不要交叉使用,否则可能会影响酶切效果。 5)酶的识别位点上的碱基被甲基化。可以选用不受甲基化影响的同裂酶,或将质粒DNA转入甲基化酶欠损的宿主菌中,重新制备DNA,也可以使用PCR的方法对DNA进行扩增,再做酶切。常用的有XbaI容易受甲基化影响,通常选用GM33做宿主菌转化。 6)底物不纯,含有限制酶阻害物质,影响酶切作用,需要重新纯化DNA。一般做乙醇沉淀纯化即可。如果质粒中含盐或酚等,都会影响酶切效果。
保护性碱基集锦
New England Biolabs Technical Literature - Updated 04/04/00 Cleavage Close to the End of DNA Fragments (oligonucleotides) To test the varying requirements restriction endonucleases have for the number of bases flanking their recognition sequences, a series of short, double-stranded oligonucleotides that contain the restriction endonuclease recognition sites (shown in red) were digested. This information may be helpful when choosing the order of addition of two restriction endonucleases for a double digest (a particular concern when cleaving sites close together in a polylinker), or when selecting enzymes most likely to cleave at the end of a DNA fragment. The experiment was performed as follows: 0.1 A 260 unit of oligonucleotide was phosphorylated using T4 polynucleotide kinase and γ-[32P] ATP. 1 μg of 5'[32P]-labeled oligonucleotide was incubated at 20°C with 20 units of restriction endonuclease in a buffer containing 70 mM Tris-HCl (pH 7.6), 10 mM MgCl 2, 5 mM DTT and NaCl or KCl depending on the salt requirement of each particular restriction endonuclease. Aliquots were taken at 2 hours and 20 hours and analyzed by 20% PAGE (7 M urea). Percent cleavage was determined by visual estimate of autoradiographs. As a control, self-ligated oligonucleotides were cleaved efficiently. Decreased cleavage efficiency for some of the longer palindromic oligonucleotides may be caused by the formation of hairpin loops .
限制性内切酶的一般原则和建议!
限制性内切酶的一般原则和建议! 1.如何做酶切反应? 该问题看似什么简单: DNA中加上酶,然后保温一段时间就可以了。但是在实际操作过程中,我们不断听到:切不动,装不上。问题在什么地方?能系列生产限制性内切酶的公司国际上,就那么几个,位列前 3 的是NEB, Fermentas, SibEnzyme。这些公司提供酶的品质一般都能得到保证。您可以怀疑酶的质量问题,但是更多的问题来源于模板是否合适酶切要求。下面几点对你的酶切是有帮助的。 1) 成功酶切的关键是准备好模板DNA。DNA样品中不能含有有机溶剂(会使酶变性或产生星号货性),不能含有干扰酶活性的污染物质,不能含有高浓度的EDTA (TE中的EDTA浓度较低,对Mg的浓度影响较小);同时要对DNA甲基化程度及其对酶切效率的影响要做到心中有数。 2) 选用合适的酶。根据酶切序列选用,特别注意选用甲基化对酶活性的干扰。 3) 正确使用和保存酶。酶需要保存在-20度的低温环境中,只是在需要用酶才从冰箱中取出来。运输和临时存放时需要将酶至于冰上。手拿酶管时不要接触酶管下步含酶的部分,移酶时尽可能用长TIP, 避免污染。用完后需要及时送回原处。注意:酶通常是最后加。所有4) 反应体积需要根据实验目的定,常规的酶切一般要维持在10-50ul,酶切鉴定10-20ul就可以了。 5) 模板浓度问题:浓度过高,溶液黏度过大,酶不能有效扩散,酶切效果不会好。浓度过低,也会影响酶活性。 6) 注意模板用量和反应体积的关系。对酶用量,模板用量,反应体积等要素的确定需要的是时间和经验的积累。 7) 酶切反应的各个组分加完后,需要用TIP小心混匀几次,short spin 一下就可以保温了。一般不能使用振荡器混匀。 8) 反应温度的选择。一般反应都用37度,但是 Sma I 的最适合温度是25度,37度时酶仍表现出活性,但是效率下降50%。部分从耐热菌制备的酶需要在37度以上的温度反应,如Taq I的最适温度为65度,37度保温,效率仅为前者的1/10。 9) 反应时间的选择。一般酶切鉴定30分钟就可以了。要完全酶切可以采用少量的酶长时间反应,或较高的酶量短时间处理都可以达到。在使用高酶量的时候需要注意甘油的最终浓度不要超过5%,也就是说10ul的体系,酶的用量不要超过1ul。 10) 是否和如何终止反应?酶切鉴定之类的实验不需要特殊处理。灭活的手段:加入高浓度的EDTA;65度或80度热处理20-30分钟;部分从高温菌纯化出来的内切酶由于最适的反应温度比较高,热处理灭活不一定完全,需要用苯酚/氯仿/乙醇方法纯化;电泳回收也是实验室常用除酶的手段。 2.如果遇到酶切不动或切不完全,该怎么办? 要回答这么问题常常需要了解酶活性单位是如何确定,我们多次接到这样的问题:1个单位的酶能在60分钟内切1ug的DNA,为什么我们的DNA那么少切那么长时间也不能切开或切完全?从下面几个因素去考虑: 1) 酶是否有活性:酶的活性单位通常是在60分钟酶切1ug lambda DNA或特定线状DNA所需要的酶量。鉴定酶的活性高低不是用您待切的DNA模板,也不是别的公司的酶来判定。因为不同公司酶可能是从不同系统中纯化的,虽然识别位点相同,但是酶的特性可能是有差异的。鉴定酶必须使用使用说明书上认定的酶活确定的方式,通常需要用lambda DAN做模板来判定。同时如果酶对甲基化敏感,还需要用Dcm-, Dam-的DNA.不排除由于运输或分装不当导致酶活性下降,这种情况是很少发生。我们公
限制性内切酶酶切位点保护碱基
限制性内切酶酶切位点 保护碱基 Document serial number【KKGB-LBS98YT-BS8CB-BSUT-BST108】
寡核苷酸近末端位点的酶切(CleavageClosetotheEndofDNAFragments(oligonucleotides)) 为了解不同内切酶对识别位点以外最少保护碱基数目的要求,NEB采用了一系列含识别序列的短双链寡核苷酸作为酶切底物进行实验。实验结果对于确定双酶切顺序将会有帮助(比如在多接头上切割位点很接近时),或者当切割位点靠近DNA末端时也很有用。在本表中没有列出的酶,则通常需在识别位点两端至少加上6个保护碱基,以确保酶切反应的进行。 实验方法:用γ-[32P]ATP在T4多聚核苷酸激酶的作用下标记0.1A 单位的寡 260 核苷酸。取1μg已标记了的寡核苷酸与20单位的内切酶,在20°C条件下分 ,5 别反应2小时和20小时。反应缓冲液含70 mMTris-HCl(pH7.6),10 mMMgCl 2 mMDTT及适量的NaCl或KCl(视酶的具体要求而定)。20%的PAGE(7 M尿素)凝胶电泳分析,经放射自显影确定酶切百分率。 本实验采用自连接的寡核苷酸作为对照。若底物有较长的回文结构,切割效率则可能因为出现发夹结构而降低。 DNA合成,新链的延伸方向是5→3因此,需要在5端加上酶切位点,因为内切酶除了有特异的识别位点之外,还需多几个无需特异性的碱基提供一个platform让它可以结合上去,否则会掉下来.引物的结构就是(5→3):保护碱基+酶切位点+原来的引物序列 首先要看目的基因中是否含有该酶切位点,只有没有的才可以选(小虾米酶切位点分析)。其次,如果需要做表达,需要考虑起始密码子,防止移码突变
各种酶切位点的保护碱基引物设计必看
各种酶切位点的保护碱基引物设计必看 Document serial number【KK89K-LLS98YT-SS8CB-SSUT-SST108】
各种酶切位点的保护碱基酶不同,所需要的酶切位点的保护碱基的数量也不同。一般情况下,在酶切位点以外多出3个碱基即可满足几乎所有限制酶的酶切要求。在资料上查不到的,我们一般都随便加3个碱基做保护。 寡核苷酸近末端位点的酶切 (Cleavage Close to the End of DNA Fragments (oligonucleotides) 为了解不同内切酶对识别位点以外最少保护碱基数目的要求,NEB采用了一系列含识别序列的短双链寡核苷酸作为酶切底物进行实验。实验结果对于确定双酶切顺序将会有帮助(比如在多接头上切割位点很接近时),或者当切割位点靠近DNA末端时也很有用。在本表中没有列出的酶,则通常需在识别位点两端至少加上6个保护碱基,以确保酶切反应的进行。 实验方法:用γ-[32P]ATP在T4多聚核苷酸激酶的作用下标记0.1A260单位的寡核苷酸。取1 μg 已标记了的寡核苷酸与20单位的内切酶,在20°C条件下分别反应2小时和20小时。反应缓冲液含70 mM Tris-HCl (pH , 10 mM MgCl2 , 5 mM DTT及适量的NaCl或KCl(视酶的具体要求而定)。20%的PAGE(7 M尿素)凝胶电泳分析,经放射自显影确定酶切百分率。 本实验采用自连接的寡核苷酸作为对照。若底物有较长的回文结构,切割效率则可能因为出现发夹结构而降低。
2.双酶切的问题 参看目录,选择共同的buffer。其实,双酶切选哪种buffer是实验的结果,takara公司从1979年开始生产限制酶以来,做了大量的基础实验,也积累了很多经验,目录中所推荐的双酶切buffer完全是依据具体实验结果得到的。 有共同buffer的,通常按照常规的酶切体系,在37℃进行同步酶切。但BamH I在37℃下有时表现出star活性,常用30℃单切。 两个酶切位点相邻或没有共同 buffer的,通常单切,即先做一种酶切,乙醇沉淀,再做另一种酶切。 3.酶切底物DNA,切不开 1)底物DNA上没有相应的限制酶识别位点,或酶切位点被甲基化。 2)PCR引物的酶切位点前没有保护碱基或引物合成有误,致使没有正确的酶切位点存在。PCR产物酶切前尽量进行精制以更换buffer。由于PCR产物中带入的其它物质,会影响酶切,据报道,通常PCR产物的添加量占总反应体积25%以下没有问题。3)酶切条件的确认,包括反应温度和反应体系等。同样的DNA,同样量,用不同的限制酶切情况可能不同,由于DNA的空间结构造成的。同样的DNA,不同的反应体系,酶切效果也可能不同,由于一些空间因素或不可测因素造成的。
常见限制性内切酶识别序列(酶切位点)
The Type II restriction systems typically contain individual restriction enzymes and modification enzymes encoded by separate genes. The Type II restriction enzymes typically recognize specific DNA sequences and cleave at constant positions at or close to that sequence to produce 5-phosphates and 3-hydroxyls. Usually they require Mg 2+ ions as a cofactor, although some have more exotic requirements. The methyltransferases usually recognize the same sequence although some are more promiscuous. Three types of DNA methyltransferases have been found as part of Type II R-M systems forming either C5-methylcytosine, N4-methylcytosine or N6-methyladenine. ApaI (类型:Type II restriction enzyme )识别序列:5'GGGCC^C 3' BamHI(类型:Type II restriction enzyme )识别序列:5' G^GATCC 3' BglII (类型:Type II restriction enzyme )识别序列:5' A^GATCT 3' EcoRI (类型:Type II restriction enzyme )识别序列:5' G^AATTC 3' HindIII (类型:Type II restriction enzyme )识别序列:5' A^AGCTT 3' KpnI (类型:Type II restriction enzyme )识别序列:5' GGTAC^C 3' NcoI (类型:Type II restriction enzyme )识别序列:5' C^CATGG 3' NdeI (类型:Type II restriction enzyme )识别序列:5' CA^TATG 3' NheI (类型:Type II restriction enzyme )识别序列:5' G^CTAGC 3' NotI (类型:Type II restriction enzyme )识别序列:5' GC^GGCCGC 3' SacI (类型:Type II restriction enzyme )识别序列:5' GAGCT^C 3' SalI (类型:Type II restriction enzyme )识别序列:5' G^TCGAC 3' SphI (类型:Type II restriction enzyme )识别序列:5' GCATG^C 3' XbaI (类型:Type II restriction enzyme )识别序列:5' T^CTAGA 3' XhoI (类型:Type II restriction enzyme )识别序列:5' C^TCGAG 3' 当然,上面总结的这些肯定不全,要查找更多内切酶的识别序列,你还可以选择下面几种方法: 1. 查你所使用的内切酶的公司的目录或者网站;NEB网站上提供的识别序列图表下载 2. 用软件如:Primer Premier5.0或Bioedit等,这些软件均提供了内切酶识别序列的信息;
保护性碱基
Cleavage Close to the End of DNA Fragments (oligonucleotides) To test the varying requirements restriction endonucleases have for the number of bases flanking their recognition sequences, a series of short, double-stranded oligonucleotides that contain the restriction endonuclease recognition sites (shown in red) were digested. This information may be helpful when choosing the order of addition of two restriction endonucleases for a double digest (a particular concern when cleaving sites close together in a polylinker), or when selecting enzymes most likely to cleave at the end of a DNA fragment. The experiment was performed as follows: 0.1 A260 unit of oligonucleotide was phosphorylated using T4 polynucleotide kinase and -[32P] ATP. 1 μg of 5′[32P]-labeled oligonucleotide was incubated at 20°C with 20 units of restriction endonuclease in a buffer containing 70 mM Tris-HCl (pH 7.6), 10 mM MgCl2, 5 mM DTT and NaCl or KCl depending on the salt requirement of each particular restriction endonuclease. Aliquots were taken at 2 hours and 20 hours and analyzed by 20% PAGE (7 M urea). Percent cleavage was determined by visual estimate of autoradiographs. As a control, self-ligated oligonucleotides were cleaved efficiently. Decreased cleavage efficiency for some of the longer palindromic oligonucleotides may be caused by the formation of hairpin loops.
常见限制性内切酶识别序列
常见限制性内切酶识别序列(酶切位点)(BamHI、EcoRI、HindIII、NdeI、 XhoI等) Time:2009-10-22 PM 15:38Author:bioer Hits: 7681 times 在分子克隆实验中,限制性内切酶是必不可少的工具酶。 无论是构建克隆载体还是表达载体,要根据载体选择合适的内切酶(当然,使用T 载就不必考虑了)。先将引物设计好,然后添加酶切识别序列到引物5' 端。常用的内切酶比如BamHI、EcoRI、HindIII、NdeI、XhoI等可能你都已经记住了它们的识别序列,不过为了保险起见,还是得查证一下。 下面是一些常用的II型内切酶的识别序列,仅供参考。先介绍一下什么是II型内切酶吧。 The Type II restriction systems typically contain individual restriction enzymes and modification enzymes encoded by separate genes. The Type II restriction enzymes typically recognize specific DNA sequences and cleave at constant positions at or close to that sequence to produce 5-phosphates and 3-hydroxyls. Usually they require Mg 2+ ions as a cofactor, although some have more exotic requirements. The methyltransferases usually recognize the same sequence although some are more promiscuous. Three types of DNA methyltransferases have been found as part of Type II R-M systems forming either C5-methylcytosine, N4-methylcytosine or N6-methyladenine. 酶类型识别序列 ApaI Type II restriction enzyme 5'GGGCC^C 3' BamHI Type II restriction enzyme 5' G^GATCC 3' BglII Type II restriction enzyme 5' A^GATCT 3' EcoRI Type II restriction enzyme 5' G^AATTC 3' HindIII Type II restriction enzyme 5' A^AGCTT 3'
保护碱基
首先要明确什么是保护碱基 限制性内切酶识别特定的DNA序列,除此之外,酶蛋白还要占据识别位点两边的若干个碱基,这些碱基对内切酶稳定的结合到DNA双链并发挥切割DNA作用是有很大影响的,被称为保护碱基。 添加保护碱基的目的 在分子克隆实验中,有时我们会在待扩增的目的基因片段两端加上特定的酶切位点,用于后续的酶切和连接反应。但实验证明,大多数限制酶对裸露的酶切位点不能切断。必须在酶切位点旁边加上一个至几个保护碱基,才能使所定的限制酶对其识别位点进行有效切断。因此在设计PCR引物时,为保护5` 端 外加的内切酶识别位点,人为地在酶切位点序列的5‘端外侧添加额外的碱基序列,即保护碱基,用来提高酶切时的活性,使酶切完全。 其次,在分子克隆实验中选择载体的酶切位点时,相临的两个酶切位点往往不能同时使用,因为一个位点切割后留下的碱基过少以至于影响旁边的酶切位点切割。 添加保护碱基的原则 添加保护碱基,需要考虑两个因素:一是碱基数目,一是碱基种类。 添加保护碱基时,最关心的应该是保护碱基的数目,而不是种类。什么样的酶切位点,添加几个保护碱基,是有数据可以参考的。 一般情况下,普通的内切酶只加入两个保护碱基,其内切反应就可以正常进行;而有一类,仅仅只加入两个保护碱基,其内切反应就不能正常进行,这是因为内切酶不能正常结合DNA段上。如NdeI就属这类,需要加入至少6个 保护碱基,常用的HindIII也要三个。 添加什么保护碱基,如果严格点,是根据两条引物的Tm值和各引物的碱基分布及GC含量。如果某条引物Tm值偏小,GC%较低,添加时多加G或C,反之亦反。 为了解不同内切酶对识别位点以外最少保护碱基数目的要求,NEB采 用了一系列含识别序列的短双链寡核苷酸作为酶切底物进行实验。实验结果对于确定双酶切顺序将会有帮助(比如在多接头上切割位点很接近时),或者当切割位点靠近DNA末端时也很有用。在本表中没有列出的酶,则通常需在识别位点两端至少加上6个保护碱基,以确保酶切反应的进行。 当在引物5’端添加酶切位点时要考虑: a)该目的序列内部不得含有相同的酶切位点,这样的错误会给将来的克隆造成麻烦。 b)如果打算PCR 后直接酶切,不要忘了在酶切位点的外侧再加上保护碱基,不同的酶对于保护碱基的要求是不同的。
关于保护碱基
关于保护碱基 1.首先要明确什么是保护碱基 限制性内切酶识别特定的DNA序列,除此之外,酶蛋白还要占据识别位点两边的若干个碱基,这些碱基对内切酶稳定的结合到DNA双链并发挥切割DNA 作用是有很大影响的,被称为保护碱基。 2.添加保护碱基的目的 在分子克隆实验中,有时我们会在待扩增的目的基因片段两端加上特定的酶切位点,用于后续的酶切和连接反应。但实验证明,大多数限制酶对裸露的酶切位点不能切断。必须在酶切位点旁边加上一个至几个保护碱基,才能使所定的限制酶对其识别位点进行有效切断。因此在设计PCR引物时,为保护5` 端外加的内切酶识别位点,人为地在酶切位点序列的5‘端外侧添加额外的碱基序列,即保护碱基,用来提高酶切时的活性,使酶切完全。 其次,在分子克隆实验中选择载体的酶切位点时,相临的两个酶切位点往往不能同时使用,因为一个位点切割后留下的碱基过少以至于影响旁边的酶切位点切割。 3.添加保护碱基的原则 添加保护碱基,需要考虑两个因素:一是碱基数目,一是碱基种类。添加保护碱基时,最关心的应该是保护碱基的数目,而不是种类。什么样的酶切位点,添加几个保护碱基,是有数据可以参考的。 一般情况下,普通的内切酶只加入两个保护碱基,其内切反应就可以正常进行;而有一类,仅仅只加入两个保护碱基,其内切反应就不能正常进行,这是因为内切酶不能正常结合DNA段上。如NdeI就属这类,需要加入至少6个保护碱基,常用的HindIII也要三个。 添加什么保护碱基,如果严格点,是根据两条引物的Tm值和各引物的碱基分布及GC含量。如果某条引物Tm值偏小,GC%较低,添加时多加G或C,反之亦反。 为了解不同内切酶对识别位点以外最少保护碱基数目的要求,NEB采用了一系列含识别序列的短双链寡核苷酸作为酶切底物进行实验。实验结果对于确定双酶切顺序将会有帮助(比如在多接头上切割位点很接近时),或者当切割位点靠
酶切位点的保护碱基原则
1 bp 2 bp 3 bp 4 bp 5 bp AciI- + + ++ +++ AgeI+++ +++ +++ +++ +++ AgeI-HF?++ +++ +++ +++ +++ AluI- +++ +++ +++ +++ ApaI+++ +++ +++ +++ +++ AscI+++ +++ +++ +++ +++ AvrII++ ++ +++ +++ +++ Enzyme Back to top Base Pairs from end 1 bp 2 bp 3 bp 4 bp 5 bp BamHI+ ++ +++ +++ +++ BamHI-HF?+ + +++ +++ +++ BglII++ +++ +++ +++ +++ BmtI+++ +++ +++ +++ +++ BmtI-HF?+++ +++ +++ +++ +++ BsaI+++ +++ +++ +++ +++ BsaI-HF?+++ +++ +++ +++ +++ BsiWI++ +++ +++ +++ +++ BsmBI+++ +++ +++ +++ +++ BsrGI+++ +++ +++ +++ +++ BssHII+ +++ +++ +++ +++
1 bp 2 bp 3 bp 4 bp 5 bp ClaI- - + +++ +++ Enzyme Back to top Base Pairs from end 1 bp 2 bp 3 bp 4 bp 5 bp DdeI+++ +++ +++ +++ +++ DpnI- ++ ++ nt nt DraIII+++ +++ +++ +++ +++ DraIII-HF?+++ +++ +++ +++ +++ Enzyme Back to top Base Pairs from end 1 bp 2 bp 3 bp 4 bp 5 bp EagI++ +++ +++ +++ +++ EagI-HF?+ +++ +++ +++ +++ EcoRI+ + ++ ++ +++ EcoRI-HF?+ + ++ +++ +++ EcoRV++ ++ ++ ++ +++ EcoRV-HF?+ ++ ++ ++ +++ Enzyme Back to top Base Pairs from end 1 bp 2 bp 3 bp 4 bp 5 bp FseI+ ++ +++ +++ +++ Enzyme Back to top Base Pairs from end 1 bp 2 3 4 5 bp
NEB保护碱基-各种酶切位点保护碱基
PCR设计引物时酶切位点的保护 酶寡核苷酸序列 切割率% 2 hr20 hr Acc I G GTCGAC C CG GTCGAC CG CCG GTCGAC CGG 0 Afl III C ACATGT G CC ACATGT GG CCC ACATGT GGG >90 >90 >90 >90 Asc I GGCGCGCC A GGCGCGCC T TT GGCGCGCC AA >90 >90 >90 >90 >90 >90 Ava I C CCCGGG G CC CCCGGG GG TCC CCCGGG GGA 50 >90 >90 >90 >90 >90 BamH I C GGATCC G CG GGATCC CG CGC GGATCC GCG 10 >90 >90 25 >90 >90 Bgl II C AGATCT G GA AGATCT TC GGA AGATCT TCC 75 25 >90 >90 BssH II G GCGCGC C AG GCGCGC CT TTG GCGCGC CAA 50 >90 BstE II G GGT(A/T)ACC C010 BstX I AACTGCAGAA CCAATGCATTGG AAAACTGCAG CCAATGCATTGG AA CTGCAGAA CCAATGCATTGG ATGCAT 25 25 50 >90 Cla I C ATCGAT G G ATCGAT C CC ATCGAT GG CCC ATCGAT GGG >90 50 >90 50
EcoR I G GAATTC C CG GAATTC CG CCG GAATTC CGG >90 >90 >90 >90 >90 >90 Hae III GG GGCC CC AGC GGCC GCT TTGC GGCC GCAA >90 >90 >90 >90 >90 >90 Hind III C AAGCTT G CC AAGCTT GG CCC AAGCTT GGG 10 75 Kpn I G GGTACC C GG GGTACC CC CGG GGTACC CCG >90 >90 >90 >90 Mlu I G ACGCGT C CG ACGCGT CG 25 50 Nco I C CCATGG G CATG CCATGG CATG 50 75 Nde I C CATATG G CC CATATG GG CGC CATATG GCG GGGTTT CATATG AAACCC GGAATTC CATATG GAATTCC GGGAATTC CATATG GAATTCCC 75 75 >90 >90 Nhe I G GCTAGC C CG GCTAGC CG CTA GCTAGC TAG 10 10 25 50 Not I TT GCGGCCGC AA ATTT GCGGCCGC TTTA AAATAT GCGGCCGC TATAAA ATAAGAAT GCGGCCGC TAAACTAT AAGGAAAAAA GCGGCCGC AAAAGGAAAA 10 10 25 25 10 10 90 >90 Nsi I TGC ATGCAT GCA CCA ATGCAT TGGTTCTGCAGTT 10 >90 >90 >90 Pac I TTAATTAA G TTAATTAA C CC TTAATTAA GG 0 25 >90
酶切位点保护碱基
本文给出了分子克隆中常用限制性内切酶的保护碱基序列,如AccI,AflIII,AscI,AvaI,BamHI,BglII,BssHII,BstEII,BstXI,ClaI,EcoRI,HaeIII,HindIII,KpnI,MluI,NcoI,NdeI,NheI,NotI,NsiI,PacI,PmeI,PstI,PvuI,SacI,SacII,SalI,ScaI,SmaI,SpeI,SphI,StuI,XbaI,XhoI,XmaI, 为什么要添加保护碱基? 在分子克隆实验中,有时我们会在待扩增的目的基因片段两端加上特定的酶切位点,用于后续的酶切和连接反应。由于直接暴露在末端的酶切位点不容易直接被限制性核酸内切酶切开,因此在设计PCR引物时,人为的在酶切位点序列的5‘端外侧添加额外的碱基序列,即保护碱基,用来提高将来酶切时的活性。 其次,在分子克隆实验中选择载体的酶切位点时,相临的两个酶切位点往往不能同时使用,因为一个位点切割后留下的碱基过少以至于影响旁边的酶切位点切割。 该如何添加保护碱基? 添加保护碱基时,最关心的应该是保护碱基的数目,而不是种类。什么样的酶切位点,添加几个保护碱基,是有数据可以参考的。 添加什么保护碱基,如果严格点,是根据两条引物的Tm值和各引物的碱基分布及GC含量。如果某条引物Tm值偏小,GC%较低,添加时多加G或C,反之亦反。 为了解不同内切酶对识别位点以外最少保护碱基数目的要求,NEB采用了一系列含识别序列的短双链寡核苷酸作为酶切底物进行实验。实验结果对于确定双酶切顺序将会有帮助(比如在多接头上切割位点很接近时),或者当切割位点靠近DNA末端时也很有用。在本表中没有列出的酶,则通常需在识别位点两端至少加上6个保护碱基,以确保酶切反应的进行。 实验方法:用γ-[32P]ATP在T4多聚核苷酸激酶的作用下标记0.1A26单位的寡核苷酸。取1μg已标记了的寡核苷酸与20单位的内切酶,在2 0 0°C条件下分别反应2小时和20小时。反应缓冲液含70mM Tris-HCl (pH 7.6), 10 mM MgCl2, 5 mMDTT及适量的NaCl或KCl(视酶的具体要求而定)。20%的PAGE(7M尿素)凝胶电泳分析,经放射自显影确定酶切百分率。 本实验采用自连接的寡核苷酸作为对照。若底物有较长的回文结构,切割效率则可能因为出现发夹结构而降低。
