2016年百川试卷柳州市专版中考全真模拟试题(一)

柳州市2016年中考全真模拟试题(一)
一.选择题(本大题共40分,每小题只有一个正确答案,每小题2分。)
1.下列属于化学变化的是()
A.镁条燃烧 B.冰雪融化 C.香水挥发 D.干冰升华
2.在溶液中含有的物质至少有()
A.一种 B.两种 C.三种 D.四种
3.食品添加剂溴酸钾(化学式:KBrO3)会致癌,其中溴元素(Br)的化合价为()
A.+1 B.+3 C.+5 D.无法确定
4.科学实验必须按规范进行操作,下列实验操作中规范的是()
A.取少量氯化钠B.闻药品气味C.滴加液体D.稀释浓硫酸
5.我们的生活离不开能源.下列能源属于“绿色”能源的是()
A.煤B.石油 C.太阳能D.天然气
6.下列事故的处理方法正确的是()
A.不慎碰倒了酒精灯,酒精在桌面燃烧,用水来灭火B.图书室内文字资料起火,立即用泡沫灭火器灭火
C.发生一氧化碳中毒,立即转移到通风的地方救治
D.如果浓硫酸沾到皮肤上,先用大量水冲洗,再涂上3%~5%的碳酸氢钠溶液
7.下列关于二氧化碳的说法错误的是()
A.二氧化碳是引起温室效应的主要气体之一B.大气中的二氧化碳是植物进行光合作用必需的物质
C.将二氧化碳气体通入紫色石蕊试液中,溶液变为红色D.实验室用大理石与稀硫酸反应制取二氧化碳
8.下列有关化学反应,对其反应类型的判断,正确的是()
①CuO+2HCl═CuCl2+H2O ②3CO+Fe2O3 2Fe+3CO2
③Cu+2AgNO3═Cu(NO3)2+2Ag ④C+CO2 2CO
A.①分解反应B.②置换反应C.③复分解反应 D.④化合反应
9.下列做法不符合环保理念的是()
A.秸秆回收利用,不露天焚烧B.预防传染病,不回收塑料制品
C.禁止在公共场所吸烟D.提倡使用太阳能热水器
10.《食品安全法》规定:食品添加剂要符合食品品质以及防腐、保鲜的要,又要对人体健康没有危害.下列做法符合规定的是()
A.将“塑化剂”添加到饮料中B.用甲醛溶液浸泡海产品
C.用回收加工后的地沟油烹制食品D.用小苏打作发酵粉焙制糕点
11.二甲醚(C2H60)是一种清洁燃料,能替代柴油作车用能源,具有广阔的市场前景.下列有关二甲醚的说法错误的是()A.由C、H、0三种元素组成B.一个分子中含有8个原子
C.相对分子质量为46 D.属于有机化合物
12.下列对分子、原子、离子的认识,正确的是()
A.只有分子是不断运动的B.原子得到或失去电子后形成离子
C.原子是最小的粒子,不可再分D.CO2和CO性质的差异主要是由于分子间的间隔不同
13.只根据电解水的实验结果,还不能得出的结论是()
A.水由氢、氧元素组成B.水分子由氢、氧原子构成
C.通电条件下,水能发生分解反应D.一个水分子由两个氢原子和一个氧原子构成
14.在配制l0%NaCl溶液的过程中,导致溶液中NaCl质量分数小于l0%的可能的原因是:
①用量筒量取水时仰视读数②配制溶液时烧杯用少量蒸馏水润洗
③在托盘天平的左盘称量氯化钠时,游码不在零位置就调节天平平衡,后将游码移动得到读数④盛装溶液的试剂瓶用蒸馏水润洗⑤氯化钠晶体不纯()
A.①②③④⑤B.只有①②④⑤C.只有①②③D.只有②③④⑤
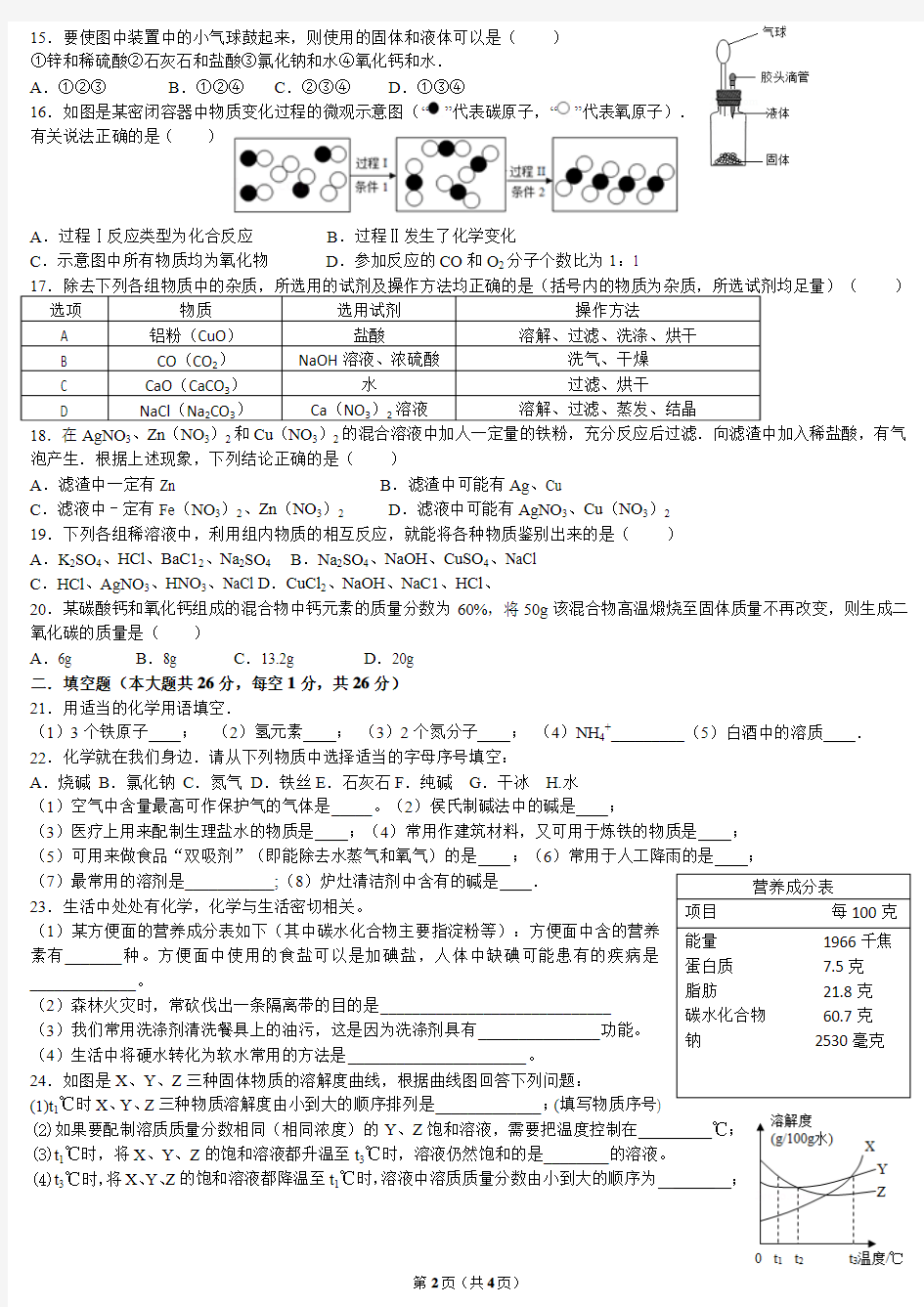
15.要使图中装置中的小气球鼓起来,则使用的固体和液体可以是( ) ①锌和稀硫酸②石灰石和盐酸③氯化钠和水④氧化钙和水. A .①②③
B .①②④
C .②③④
D .①③④
16.如图是某密闭容器中物质变化过程的微观示意图(“”代表碳原子,“”代表氧原子).
有关说法正确的是( )
A .过程Ⅰ反应类型为化合反应
B .过程Ⅱ发生了化学变化
C .示意图中所有物质均为氧化物
D .参加反应的CO 和O 2分子个数比为1:1
) 18.在AgNO 3、Zn (NO 3)2和Cu (NO 3)2的混合溶液中加人一定量的铁粉,充分反应后过滤.向滤渣中加入稀盐酸,有气泡产生.根据上述现象,下列结论正确的是( )
A .滤渣中一定有Zn
B .滤渣中可能有Ag 、Cu
C .滤液中﹣定有Fe (NO 3)2、Zn (NO 3)2
D .滤液中可能有AgNO 3、Cu (NO 3)2 19.下列各组稀溶液中,利用组内物质的相互反应,就能将各种物质鉴别出来的是( ) A .K 2SO 4、HCl 、BaC12、Na 2SO 4 B .Na 2SO 4、NaOH 、CuSO 4、NaCl C .HCl 、AgNO 3、HNO 3、NaCl D .CuCl 2、NaOH 、NaC1、HCl 、
20.某碳酸钙和氧化钙组成的混合物中钙元素的质量分数为60%,将50g 该混合物高温煅烧至固体质量不再改变,则生成二氧化碳的质量是( ) A .6g
B .8g
C .13.2g
D .20g
二.填空题(本大题共26分,每空1分,共26分) 21.用适当的化学用语填空.
(1)3个铁原子 ; (2)氢元素 ; (3)2个氮分子 ; (4)NH 4+_________(5)白酒中的溶质 . 22.化学就在我们身边.请从下列物质中选择适当的字母序号填空: A .烧碱 B .氯化钠 C .氮气 D .铁丝E .石灰石F .纯碱 G .干冰 H.水 (1)空气中含量最高可作保护气的气体是_____。(2)侯氏制碱法中的碱是 ;
(3)医疗上用来配制生理盐水的物质是 ;(4)常用作建筑材料,又可用于炼铁的物质是 ; (5)可用来做食品“双吸剂”(即能除去水蒸气和氧气)的是 ;(6)常用于人工降雨的是 ; (7)最常用的溶剂是___________;(8)炉灶清洁剂中含有的碱是 . 23.生活中处处有化学,化学与生活密切相关。
(1)某方便面的营养成分表如下(其中碳水化合物主要指淀粉等):方便面中含的营养素有_______种。方便面中使用的食盐可以是加碘盐,人体中缺碘可能患有的疾病是_____________。
(2)森林火灾时,常砍伐出一条隔离带的目的是_____________________________ (3)我们常用洗涤剂清洗餐具上的油污,这是因为洗涤剂具有_______________功能。 (4)生活中将硬水转化为软水常用的方法是______________________。 24.如图是X 、Y 、Z 三种固体物质的溶解度曲线,根据曲线图回答下列问题:
(1)t 1℃时X 、Y 、Z 三种物质溶解度由小到大的顺序排列是_____________;(填写物质序号)
(2)如果要配制溶质质量分数相同(相同浓度)的Y 、Z 饱和溶液,需要把温度控制在_________℃; (3)t 1℃时,将X 、Y 、Z 的饱和溶液都升温至t 3℃时,溶液仍然饱和的是
________的溶液。
(4)t 3℃时,将X 、Y 、Z 的饱和溶液都降温至t 1℃时,溶液中溶质质量分数由小到大的顺序为 _____ ;
25.氢氧化钠和氢氧化钙是两种常见的碱.李红同学将两种碱的溶液分别装入试管A、B中,并进行了如图所示的三组实验.
(1)实验l 中,两支试管的溶液都变成色.
(2)实验2中,若B 盛装的是NaOH 溶液,发生反应的化学方程式为:___________________.
(3)实验3中,李红同学向两支试管吹气,B中无现象,吹气后B中的溶质可能是下列中的:.
A.只有NaOH
B.NaOH Na2CO3
C.只有Na2CO3
D.H2CO3NaOH
(4)欲验证B 中溶质的成分,应选择的试剂是_____________。
A.酚酞溶液
B.稀盐酸
C.BaCl2溶液和酚酞溶液
D.Ba(OH)2溶液和酚酞溶液
三、简答题(本大题共12分,每空1分)
26.在元素周期表的指导下,利用元素之间的一些规律性知识来分类学习物质的性质,就使化学学习和研究变得有规律可循.如图1所示是元素周期表的一部分.
(1)硅元素的相对原子质量为_______________________ 。
(2)第三周期中具有相对稳定结构的原子的原子序数为_______
(3)写出地壳中含量最多的金属元素和非金属元素与16号元素组成的化合物的化学式_____.
(4)如图2所示的微粒中,属于同种元素的是(填序号),元素的化学性质相似的是.(填序号)
27.Na2SO4是制造纸张、药品、染料稀释剂的重要原料.某Na2SO4样品中含有少量CaCl2和MgCl2,实验室提纯Na2SO4的流程如图甲所示.
(1)加入NaOH溶液主要除去的阳离子是(填离子符号),其反应的化学方程式为.
(2)若加入的NaOH溶液和Na2CO3溶液都过量,可在后续的流程中加入适量的_____(填名称)除去.
(3)操作a的名称是____,该操作中需要用到的玻璃仪器有烧杯、玻璃棒、___.
(4)若溶液M中的溶质是Na2SO4和NaCl,根据图乙的溶解度曲线可知,操作b应为:先将溶液M,再降温结晶、过滤.降温结晶的最佳温度范围是℃以下,这是因为.
28.实验室现有氯酸钾、二氧化锰、石灰石、蜡烛、火柴及以下仪器(如图1):
请回答:
(1)仪器⑦的名称是;
(2)若补充一种常用仪器(填名称),并利用上述部分仪器和药品可制取一种气体,该反应的化学方程式是;
(3)若补充一种药品,还能制取二氧化碳,并探究其性质(如图2):
①补充的药品是;
②图2中A观察到的现象是,B中可用来测量生成二氧化碳气体的体积,其中在水面上放一层植物油的原因是.
(4)某同学设计如图所示的装置用于分离H2和CO2的混合气体.按照实验规范操作,在导管口最后收集到的气体是__________(选填下列选项)。
A.O2
B.CO2
C.O2和CO2
D.CO2和O2
29.某学习小组探究氢氧化钙溶液的化学性质,并作了延伸探究.
澄清石灰水变浑浊红色褪为无色
【提出问题】实验方案(3)褪色后溶液中的溶质是什么?
【查阅资料】CaCl2溶液呈中性.
【作出猜想】乙同学从反应情况分析,溶液中除含少量酚酞外,溶质可能有以下三种情况:
①CaCl2;②__________________________ ③CaCl2和Ca(OH)2
【分析讨论】丙同学从实验现象分析得出:猜想_______肯定不合理,其理由是.
探究二:丁同学为进一步验证乙同学的猜想,设计实验如下:将实验方案(3)褪色后溶液倒入烧杯中,向其中逐滴滴加稀碳酸钠溶液至过量,边滴边振荡.实验后得出产生沉淀质量与滴加碳酸钠溶液体积之间的关系,如图所示.写出实验过程中的现象.
【得出结论】乙同学的猜想中,(填序号)合理.
【反思讨论】
学习小组结合图象,分析了丁同学实验过程中烧杯内溶液的变化.下列说法正确的是.(填序号)A.溶液质量逐渐增大B.氯化钠质量逐渐增大,V2后不变
C.氯化钙的质量先增大后减小D.溶液的pH一直在增大.
30.为了测定某含杂质7%的黄铜样品中铜的质量分数(杂质中不含铜、锌元素,杂质不溶于
水,不与其它物质反应,受热也不分解),某化学小组进行了如下实验.计算:
(1)盐酸中溶质的各元素的原子个数比为_______________。
(2)该黄铜样品中铜的质量分数?(要求写出计算过程)
(3)向过滤后所得滤液中加入87.4g水,则最终所得溶液中溶质的质量分数是____________。
(4)配制上述质量分数为14.6%的稀盐酸,需要质量分数为36.5%的浓盐酸的质量为_____。
(5)欲将黄铜样品中的铜转化为铜盐,可将过滤后所得的不溶性物质洗涤、烘干,然后在空气中加热,充分反应,则可得到含杂质的氧化铜的质量是,在经过某些反应及操作就得到了所需铜盐.
